Additifs pour l'alimentation animale : Autorisations de janvier-février 2024
- Feed additives
- Feed safety
Résumé
Une vue d'ensemble des dernières autorisations, réautorisations et refus d'autorisation des additifs pour l'alimentation animale et de leur utilisation dans l'alimentation des animaux cibles.
L'UE autorise ou réautorise certains additifs pour l'alimentation animale et refuse d'autres autorisations
Règlements d'application de la Commission 2024/220, 2024/221, 2024/228, 2024/231, 2024/239, 2024/251, 2024/252, 2024/260, 2024/261, 2024/262, 2024/265, 2024/285, 2024/749, 2024/750, 2024/752, 2024/754, 2024/763
Mise à jour
Une vue d'ensemble des dernières autorisations, réautorisations et refus d'autorisation des additifs pour l'alimentation animale et de leur utilisation dans l'alimentation des animaux cibles.
Produits concernés
Additifs pour l'alimentation animale, fourrages préparés
qu'est-ce qui change ?
Nouvelles autorisations (janvier - février 2024)
En janvier et février 2024, l'UE a autorisé les nouveaux additifs pour l'alimentation animale énumérés dans le tableau 1.
Ces autorisations sont basées sur les avis suivants publiés par l'Autorité européenne de sécurité des aliments : EFSA(2022a),(2022b),(2022c), (2022d),(2022e),(2023a),(2023b),(2023c),(2023d),(2023e),(2023f),(2023g),(2023h),(2023i).
Réautorisations
En janvier et février 2024, l'UE a réautorisé les additifs pour l'alimentation animale énumérés dans le tableau 2.
Ces réautorisations sont basées sur les avis suivants publiés par l'EFSA :(2023j), (2023k),(2023l),(2023m),(2023n),(2023o),(2023p), (2023q).
Autorisations refusées
Le règlement 2024/752 refuse l'autorisation d'une préparation de Phaffia rhodozyma (ATCC SD-5340) riche en astaxanthine en tant qu'additif alimentaire pour le saumon et la truite, sur la base de l'avis de l'EFSA(2022f).
Autorisations modifiées
Le règlement 2024/754 autorise l'utilisation d'une préparation de Bacillus subtilis DSM 32324, DSM 32325 et Bacillus amyloliquefaciens DSM 25840 pour toutes les espèces de volailles simultanément avec les coccidiostatiques diclazuril, décoquinate, halofuginone, monensine, salinomycine, narasin, une combinaison de nicarbazine et de narasin, et lasalocide, sur la base de l'avis de l'EFSA(2023r) selon lequel ces utilisations sont compatibles.
L'UE a également corrigé et modifié les règlements d'exécution (UE) 2022/1421, (UE) 2022/652, (UE) 2022/1490 et (UE) 2022/320 concernant l'utilisation d'huile essentielle d'orange exprimée, d'huile essentielle d'orange distillée et d'huiles d'orange repliées de Citrus sinensis en tant qu'additifs pour l'alimentation des chiens, des chats, des chevaux, des lapins, des poissons d'ornement et des oiseaux d'ornement.
pourquoi ?
Les demandes d'autorisation et de renouvellement d'autorisation susmentionnées ont été soumises et examinées par le laboratoire de référence institué par le règlement sur les additifs pour l'alimentation animale(1831/2003).
L'EFSA n'a pas été en mesure de se prononcer sur la sécurité de Phaffia rhodozyma (ATCC SD-5340), riche en astaxanthine, en tant qu'additif alimentaire pour le saumon et la truite, ni sur sa sécurité pour les consommateurs de ces produits.
L'EFSA n'a pas pu se prononcer sur la sécurité des sous-produits d'agrumes en tant qu'additifs alimentaires pour les chiens, les chats et les poissons d'ornement, car ces animaux ne sont pas normalement exposés à ces sous-produits.
Calendrier
Les règlements 2024/220, 2024/221, 2024/228, 2024/231 et 2024/260 s'appliquent à partir du 1er février 2024. Ces autorisations restent valables jusqu'au 4 février 2034.
Les règlements 2024/251, 2024/252 et 2024/285 s'appliquent à partir du 6 février 2024. Ces autorisations restent valables jusqu'au 6 février 2034.
Les règlements 2024/261, 2024/262, 2024/265 et 2024/285 s'appliquent à partir du 7 février 2024. Ces autorisations restent valables jusqu'au 7 février 2034.
Les règlements 2024/749, 2024/750, 2024/752, 2024/754 et 2024/763 s'appliquent à partir du 21 mars 2024. Ces autorisations restent valables jusqu'au 21 mars 2034.
quelles sont les principales implications pour les pays exportateurs ?
Grâce aux nouvelles autorisations, davantage d'additifs pour l'alimentation animale seront disponibles sur le marché. Les autorisations et les renouvellements sont valables 10 ans. Le mode d'utilisation de toutes les préparations et substances spécifiées en tant qu'additifs pour l'alimentation animale doit être conforme aux dispositions d'utilisation spécifiées dans l'annexe de chaque règlement.
Actions recommandées
Il est recommandé aux pays non membres de l'UE qui produisent des additifs pour l'alimentation animale, des aliments composés pour animaux et des matières premières pour l'alimentation animale destinés à être exportés vers l'UE de vérifier le statut des additifs pour l'alimentation animale dans le registre des additifs pour l'alimentation animale de l'UE.
Pour pouvoir filtrer et voir plus d'informations, il est conseillé de télécharger le registre au format Excel (voir le pied du portail d'information sur les denrées alimentaires et les aliments pour animaux).
Contexte
La procédure d'autorisation de mise sur le marché et d'utilisation des additifs pour l'alimentation animale est définie dans le règlement (CE) 1831/2003. Pour obtenir les dernières mises à jour sur les additifs pour l'alimentation animale, consultez le registre des additifs pour l'alimentation animale de l'UE.
Ressources
Commission européenne :
Règlement 1831/2003 relatif aux additifs destinés à l'alimentation des animaux
Registre des additifs pour l'alimentation animale de l'UE
Autorité européenne de sécurité des aliments :
EFSA (2023a) Efficacité d'un additif alimentaire composé de Companilactobacillus farciminis CNCM I-3740 (Biacton®) pour poulets et dindes d'engraissement (ChemVet dk A/S). EFSA Journal, 21(6) : 8049.
EFSA (2023b) Sécurité et efficacité d'un additif alimentaire composé de bromhydrate d'halofuginone (STENOROL®) pour les poulets d'engraissement et les dindes d'engraissement/élevées pour la reproduction. Journal de l'EFSA, 21(4) : 7978.
EFSA (2023c) Sécurité et efficacité d'un additif alimentaire consistant en une teinture dérivée du fruit d 'Anethum graveolens L. (teinture d'aneth) destiné à toutes les espèces animales (FEFANA asbl). Journal de l'EFSA, 21(1) : 7691.
EFSA (2023d) Sécurité et efficacité d'un additif pour l'alimentation animale consistant en une teinture dérivée du fruit de Foeniculum vulgare Mill. ssp. vulgare var. dulce (teinture de fenouil doux) destiné à être utilisé chez toutes les espèces animales (FEFANA asbl). Journal de l'EFSA, 21(1) : 7693.
EFSA (2023e) Sécurité et efficacité d'un additif pour l'alimentation animale consistant en une teinture dérivée du fruit de Petroselinum crispum (Mill.) Fuss (teinture de persil) destiné à être utilisé chez toutes les espèces animales (FEFANA asbl). Journal de l'EFSA, 21(1) : 7694.
EFSA (2023f) Safety and efficacy of feed additives prepared from Piper nigrum L. : black pepper oil and black pepper oleoresin for use in all animal species and a supercritical extract for use in dogs and cats (FEFANA asbl). Journal de l'EFSA, 20(11) : 7599.
EFSA (2023g) Sécurité et efficacité d'un additif alimentaire consistant en un complexe zinc(II)-bétaïne pour toutes les espèces animales (Biochem Zusatzstoffe Handels- und Produktionsges. mbH). Journal de l'EFSA, 21(2) : 7819.
EFSA (2023h) Sécurité et efficacité d'un additif pour l'alimentation animale consistant en une teinture dérivée des racines d' Eleutherococcus senticosus (Rupr. & Maxim.) Maxim. (teinture de racine de taïga) pour chiens, chats et chevaux (FEFANA asbl). Journal de l'EFSA, 21(2) : 7876.
EFSA (2023i) Safety of a feed additive consisting of lignosulphonate for all animal species (Borregaard AS). EFSA Journal, 21(4) : 7956.
EFSA (2023j) Évaluation de l'additif pour l'alimentation animale composé de Pediococcus pentosaceus NCIMB 30168 pour toutes les espèces animales en vue du renouvellement de son autorisation (Volac International Ltd). EFSA Journal, 21(6) : 8046.
EFSA (2023k) Sécurité et efficacité d'un additif alimentaire composé d'endo-1,4-bêta-xylanase, d'endo-1,3(4)-bêta-glucanase et d'endo-1,4-bêta-glucanase produites par Trichoderma reesei ATCC 74444 (Ronozyme® Multigrain) destiné aux volailles d'engraissement, aux volailles de ponte et aux porcelets (sevrés) (DSM Nutritional Products). Journal de l'EFSA, 21(6) : 8043.
EFSA (2023l) Évaluation de huit additifs pour l'alimentation animale composés de Lactiplantibacillus plantarum CNCM I-3235, L. plantarum CNCM I-3736/DSM 11672, Pediococcus acidilactici CNCM I-3237, P. acidilactici CNCM I-4622/DSM 11673, Pediococcus pentosaceus NCIMB 12455, Acidipropionibacterium acidipropionici CNCM I-4661, Lentilactobacillus buchneri NCIMB 40788/CNCM I-4323 et L. buchneri NCIMB 40788/CNCM I-4323 et Lentilactobacillus hilgardii CNCM I-4785 pour toutes les espèces animales en vue du renouvellement de leur autorisation (Danstar Ferment AG). Journal de l'EFSA, 21(2) : 7865.
EFSA (2023m) Évaluation de l'additif alimentaire composé de Lactiplantibacillus plantarum DSM 23375 pour toutes les espèces animales en vue du renouvellement de son autorisation (Agri-King, Inc.). EFSA Journal, 21(6) : 8054.
EFSA (2023n) Sécurité et efficacité d'un additif alimentaire composé d'endo-1,4-β-glucanase produite par Trichoderma citrinoviride IMI 360748 (Hostazym C) destiné à toutes les espèces de volailles d'engraissement et élevées pour la ponte/l'élevage, aux oiseaux d'ornement et aux porcelets (sevrés et allaitants) (Huvepharma NV). Journal de l'EFSA, 21(4) : 7954.
EFSA (2023o) Évaluation de l'additif alimentaire composé de thaumatine pour toutes les espèces animales en vue du renouvellement de son autorisation (ADISSEO France S.A.S.). EFSA Journal, 21(6) : 8077.
EFSA (2023p) Évaluation de l'additif pour l'alimentation animale composé de Lactiplantibacillus plantarum(anciennement Lactobacillus plantarum) NCIMB 30083 pour toutes les espèces animales en vue du renouvellement de son autorisation (Chr. Hansen A/S). Journal de l'EFSA, 21(8) : 8154.
EFSA (2023q) Évaluation de l'additif alimentaire composé de Lactiplantibacillus plantarum (anciennement Lactobacillus plantarum) NCIMB 30084 pour toutes les espèces animales en vue du renouvellement de son autorisation (Chr. Hansen A/S). Journal de l'EFSA, 21(7) : 8167.
EFSA (2023r) Évaluation de la demande de modification des termes de l'autorisation de l'additif alimentaire composé de Bacillus subtilis DSM 32324, Bacillus subtilis DSM 32325 et Bacillus amyloliquefaciens DSM 25840 (GalliPro® Fit) pour toutes les espèces de volailles d'engraissement et élevées pour la ponte/la reproduction (Chr. Hansen A/S). Journal de l'EFSA, 21(8) : 8179.
EFSA (2022a) Sécurité et efficacité d'un additif alimentaire composé d'une huile essentielle du fruit de Cuminum cyminum L. (huile de cumin) pour toutes les espèces animales (FEFANA asbl). EFSA Journal, 20(12) : 7690.
EFSA (2022b) Sécurité et efficacité d'un additif alimentaire consistant en une teinture dérivée des racines d' Angelica sinensis (Oliv.) Diels (teinture de dong quai) pour utilisation chez les volailles, les chevaux, les chiens et les chats (FEFANA asbl). Journal de l'EFSA, 20(12) : 7692.
EFSA (2022c) Sécurité et efficacité d'un additif pour l'alimentation animale consistant en une teinture dérivée du fruit d 'Illicium verum Hook f. (teinture d'anis étoilé) destiné à être utilisé chez toutes les espèces animales (FEFANA asbl). Journal de l'EFSA, 20(12) : 7695.
EFSA (2022d) Sécurité et efficacité d'un additif alimentaire consistant en une huile essentielle provenant des parties aériennes d'Anethum graveolens L. (huile d'aneth) pour utilisation chez les chiens et les chats (FEFANA asbl). Journal de l'EFSA, 20(12) : 7689.
EFSA (2022e) Sécurité et efficacité d'un additif alimentaire composé d'une huile essentielle provenant de la gomme-résine de Ferula assa-foetida L. (huile d'asafoetida) pour utilisation chez les chiens et les chats (FEFANA asbl). Journal de l'EFSA, 20(12) : 7688.
EFSA (2022f) Safety and efficacy of a feed additive consisting of astaxanthin-rich Phaffia rhodozyma for salmon and trout (Igene Biotechnology, Inc.) (Sécurité et efficacité d'un additif alimentaire composé de Phaffia rhodozyma riche en astaxanthine pour le saumon et la truite). EFSA Journal, 20(2) : 7161.
Sources
Règlement d'exécution de la Commission :
2024/220 concernant le renouvellement de l'autorisation d'une préparation de Pediococcus pentosaceus NCIMB 30168 en tant qu'additif pour l'alimentation de toutes les espèces animales
2024/221 concernant le renouvellement de l'autorisation d'une préparation d'endo-1,4-bêta-xylanase, d'endo-1,3(4)-bêta-glucanase et d'endo-1,4-bêta-glucanase, produite par Trichoderma reesei ATCC 74444, en tant qu'additif pour l'alimentation de toutes les espèces de volailles d'engraissement, de toutes les espèces de volailles de ponte et des porcelets sevrés
2024/228 concernant l'autorisation d'une préparation de Companilactobacillus farciminis CNCM I-3740 en tant qu'additif alimentaire pour les poulets d'engraissement et les dindes d'engraissement
2024/231 concernant l'autorisation d'une préparation de bromhydrate d'halofuginone (Stenorol) en tant qu'additif alimentaire pour les poulets d'engraissement, les dindes d'engraissement et les dindes d'élevage
2024/239 rectifiant et modifiant les règlements d'exécution (UE) 2022/1421, (UE) 2022/652, (UE) 2022/1490 et (UE) 2022/320
2024/251 concernant le renouvellement de l'autorisation des préparations de Lactiplantibacillus plant arum CNCM I-3235, Lactiplantibacillus plantarum DSM 11672/CNCM I-3736, Pediococcus acidilactici CNCM I-3237, Pediococcus acidilactici DSM 11673/CNCM I-4622, Pediococcus pentosaceus NCIMB 12455, Acidipropionibacterium acidipropionici CNCM I-4661, Lentilactobacillus buchneri NCIMB 40788/CNCM I-4323 et Lentilactobacillus hilgardii CNCM I-4785 et Lentilactobacillus buchneri CNCM I-4323/NCIMB 40788 en tant qu'additifs pour l'alimentation de toutes les espèces animales
2024/252 concernant le renouvellement de l'autorisation d'une préparation de Lactiplantibacillus plantarum DSM 23375 en tant qu'additif pour l'alimentation de toutes les espèces animales
2024/260 concernant l'autorisation de l'huile essentielle de cumin ( Cuminum cyminum L.), de la teinture de fenouil doux ( Foeniculum vulgare Mill. ssp. vulgare var. dulce), de la teinture de dong quai ( Angelica sinensis (Oliv.) Diels), de la teinture de persil ( Petroselinum crispum (Mill.) Fuss), de la teinture d'anis étoilé ( Illicium verum Hook f., l'huile essentielle d'asafoetida de Ferula-assa-foetida L., l'huile essentielle d'aneth d'Anethum graveolens L. et la teinture d'aneth d'Anethum graveolens L. en tant qu'additifs alimentaires pour certaines espèces animales
2024/261 concernant l'autorisation de l'huile essentielle de poivre noir et de l'oléorésine de poivre noir de Piper nigrum L. en tant qu'additifs alimentaires pour toutes les espèces animales et de l'extrait supercritique de poivre noir de Piper nigrum L. en tant qu'additif alimentaire pour les chats et les chiens
2024/262 concernant le renouvellement de l'autorisation d'une préparation d'endo-1,4-bêta-glucanase produite par Trichoderma citrinoviride IMI 360748 en tant qu'additif alimentaire pour les poulets d'engraissement, les espèces mineures de volailles d'engraissement et les porcelets sevrés, l'autorisation de cette préparation en tant qu'additif alimentaire pour les dindes d'engraissement, toutes les espèces de volailles élevées pour la ponte ou la reproduction, les oiseaux d'ornement et les porcelets de lait
2024/285 concernant l'autorisation de la teinture de racine de taïga provenant de l'Eleutherococcus senticosus (Rupr. & Maxim.) Maxim en tant qu'additif alimentaire pour les chiens, les chats et les chevaux
2024/749 concernant l'autorisation du lignosulfonate en tant qu'additif alimentaire pour toutes les espèces animales
2024/750 concernant le renouvellement de l'autorisation de la thaumatine en tant qu'additif pour l'alimentation de toutes les espèces animales
2024/752 concernant le refus d'autorisation d'une préparation de Phaffia rhodozyma (ATCC SD-5340) riche en astaxanthine en tant qu'additif pour l'alimentation des saumons et des truites
2024/754 modifiant le règlement d'exécution (UE) 2020/1762 en ce qui concerne les conditions d'autorisation d'une préparation de Bacillus subtilis DSM 32324, Bacillus subtilis DSM 32325 et Bacillus amyloliquefaciens DSM 25840 en tant qu'additif pour l'alimentation de toutes les espèces de volailles d'engraissement, de ponte ou de reproduction
2024/763 concernant le renouvellement de l'autorisation des préparations de Lactiplantibacillus plant arum NCIMB 30083 et Lactiplantibacillus plantarum NCIMB 30084 en tant qu'additifs pour l'alimentation de toutes les espèces animales
Tableaux et figures
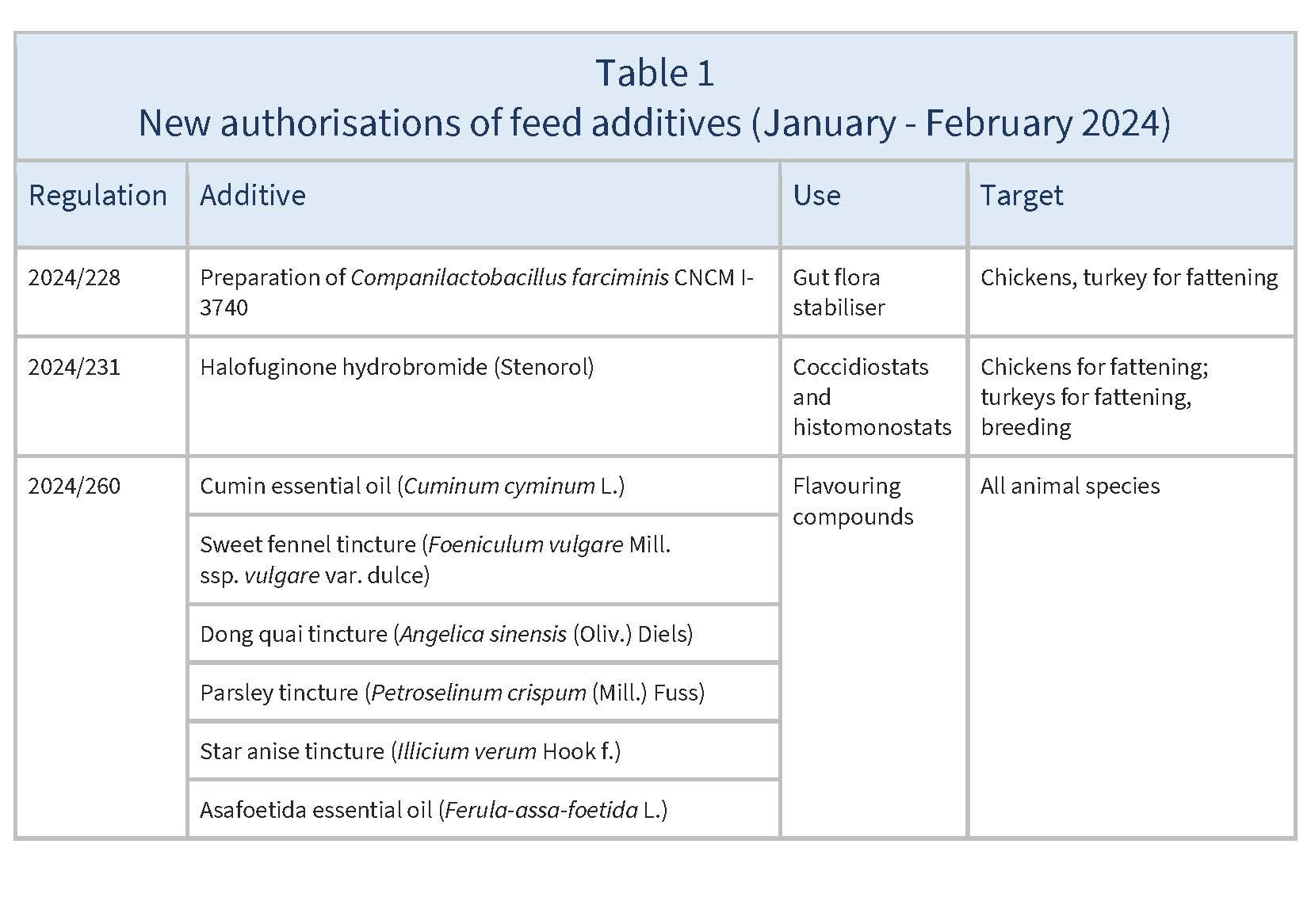
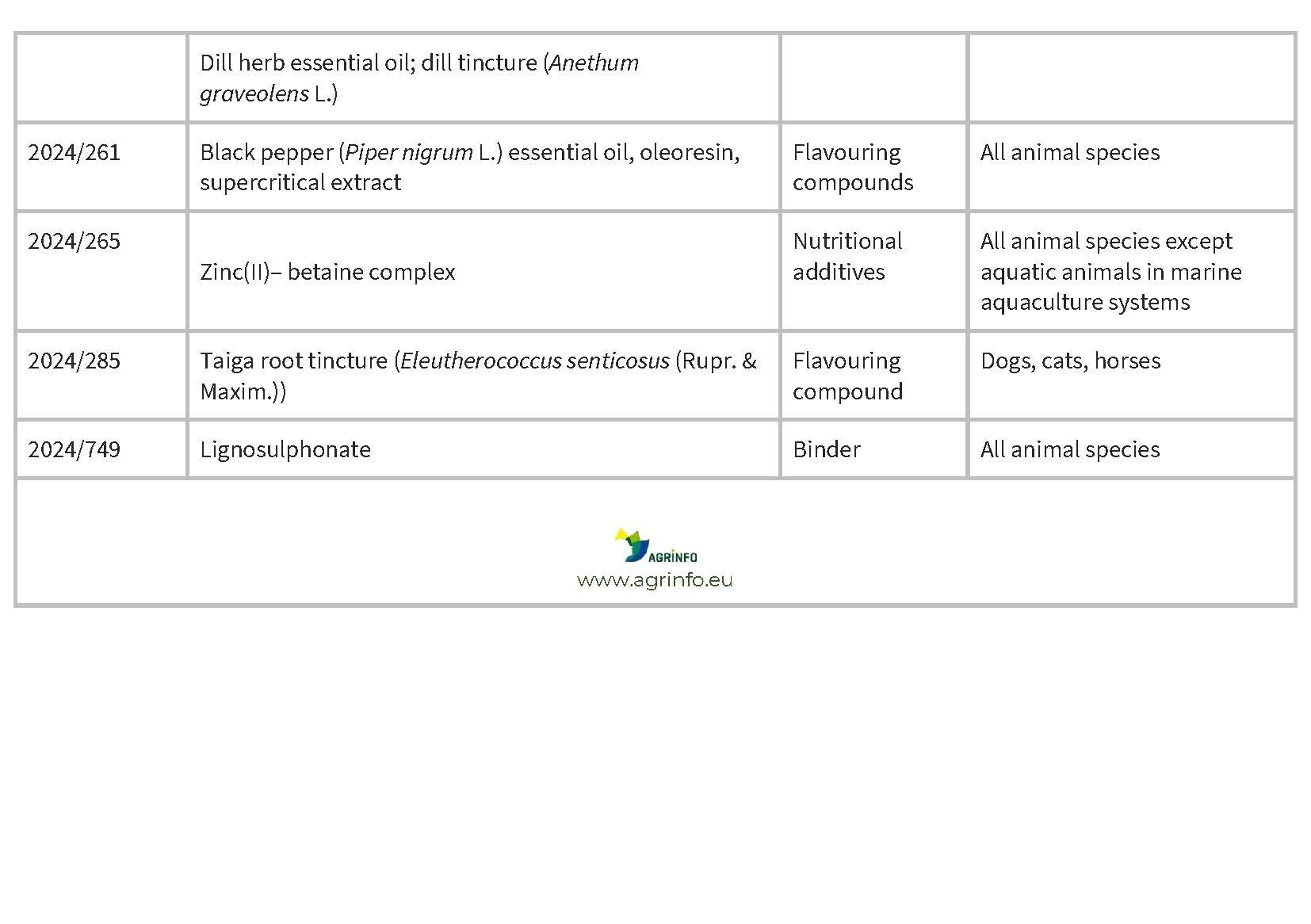
Source: based on Regulations 2024/228, 2024/231, 2024/260, 2024/261, 2024/265, 2024/285, 2024/749
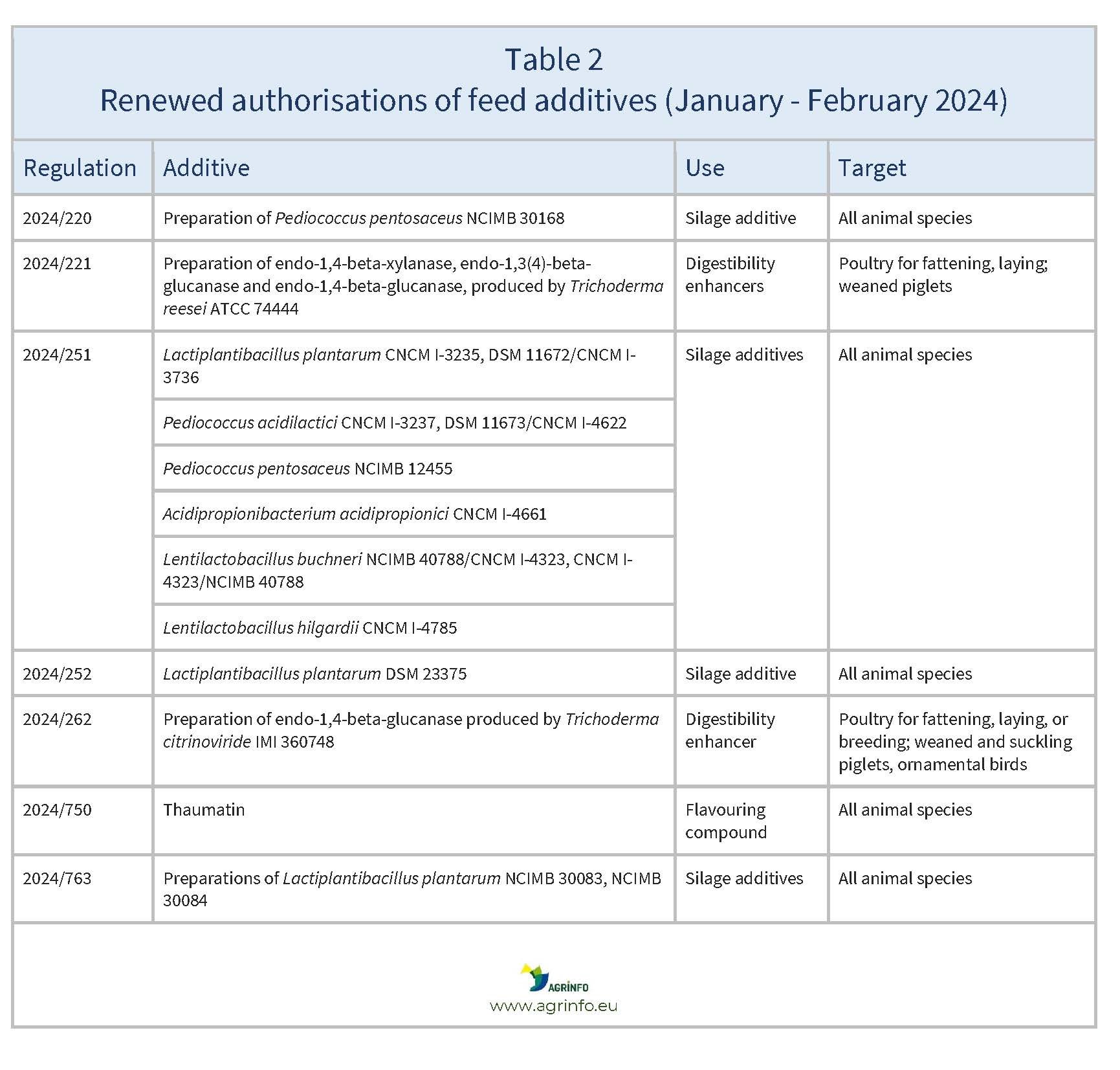
Source: based on Regulations 2024/220, 2024/221, 2024/251, 2024/252, 2024/262, 2024/750, 2024/763
Clause de non-responsabilité : COLEAD ne peut en aucun cas être tenu responsable des pertes, dommages, responsabilités ou dépenses encourus ou subis qui résulteraient de l'utilisation des informations disponibles sur ce site web ou de tout lien vers des sites externes. L'utilisation du site web se fait aux seuls risques et responsabilités de l'utilisateur. Cette plateforme d'information a été créée et maintenue avec le soutien financier de l'Union européenne. Son contenu ne reflète toutefois pas le point de vue de l'Union européenne.
L'UE autorise ou réautorise certains additifs pour l'alimentation animale et refuse d'autres autorisations
Commission Implementing Regulations 2024/220, 2024/221, 2024/228, 2024/231, 2024/239, 2024/251, 2024/252, 2024/260, 2024/261, 2024/262, 2024/265, 2024/285, 2024/749, 2024/750, 2024/752, 2024/754, 2024/763
qu'est-ce qui change et pourquoi ?
En janvier et février 2024, l'UE a autorisé les nouveaux additifs pour l'alimentation animale énumérés dans le tableau 1. Les demandes d'autorisation ont été soumises et examinées par le laboratoire de référence établi par le règlement sur les additifs pour l'alimentation animale(1831/2003).
L'UE a réautorisé les additifs pour l'alimentation animale énumérés dans le tableau 2, mais a refusé d'autoriser une préparation de Phaffia rhodozyma (ATCC SD-5340) riche en astaxanthine en tant qu'additif pour l'alimentation du saumon et de la truite, car l'Autorité européenne de sécurité des aliments (EFSA) n'a pas été en mesure de se prononcer sur sa sécurité pour les consommateurs.
L'UE autorise l'utilisation de certaines préparations de Bacillus et de certains coccidiostatiques pour les volailles, car l'EFSA estime que ces utilisations sont compatibles.
Actions
Il est recommandé aux pays non membres de l'UE qui produisent des additifs pour l'alimentation animale, des aliments composés pour animaux et des matières premières pour l'alimentation animale destinés à être exportés vers l'UE de vérifier le statut des additifs pour l'alimentation animale dans le registre des additifs pour l'alimentation animale de l'UE.
Pour pouvoir filtrer et voir plus d'informations, il est conseillé de télécharger le registre au format Excel (voir le pied du portail d'information sur les denrées alimentaires et les aliments pour animaux).
Calendrier
Les règlements 2024/220, 2024/221, 2024/228, 2024/231, 2024/260 s'appliquent à partir du 1er février 2024. Ces autorisations restent valables jusqu'au 4 février 2034.
Les règlements 2024/251, 2024/252 et 2024/285 s'appliquent à partir du 6 février 2024. Ces autorisations restent valables jusqu'au 6 février 2034.
Les règlements 2024/261, 2024/262, 2024/265 et 2024/285 s'appliquent à partir du 7 février 2024. Ces autorisations restent valables jusqu'au 7 février 2034.
Les règlements 2024/749, 2024/750, 2024/752, 2024/754 et 2024/763 s'appliquent à partir du 21 mars 2024. Ces autorisations restent valables jusqu'au 21 mars 2034.
Tableaux et figures


Source: based on Regulations 2024/228, 2024/231, 2024/260, 2024/261, 2024/265, 2024/285, 2024/749

Source: based on Regulations 2024/220, 2024/221, 2024/251, 2024/252, 2024/262, 2024/750, 2024/763
Clause de non-responsabilité : COLEAD ne peut en aucun cas être tenu responsable des pertes, dommages, responsabilités ou dépenses encourus ou subis qui résulteraient de l'utilisation des informations disponibles sur ce site web ou de tout lien vers des sites externes. L'utilisation du site web se fait aux seuls risques et responsabilités de l'utilisateur. Cette plateforme d'information a été créée et maintenue avec le soutien financier de l'Union européenne. Son contenu ne reflète toutefois pas le point de vue de l'Union européenne.
