Aditivos para piensos: Autorizaciones, reautorizaciones, retiradas y cambios de mayo a julio de 2025
- Feed additives
- Feed safety
Resumen
Panorama de las últimas autorizaciones de aditivos para piensos y su uso en nutrición animal en animales diana.
La UE autoriza determinados aditivos para piensos y retira otros
Reglamentos de aplicación de la Comisión 2025/757, 2025/1254, 2025/1386, 2025/1390, 2025/1391, 2025/1392, 2025/1395, 2025/1400, 2025/1402, 2025/1403, 2025/1417, 2025/1418, 2025/1419, 2025/1423, 2025/1424, 2025/1426, 2025/1465, 2025/1468, 2025/1504, 2025/1523, 2025/1527
Notificaciones G/SPS/N/EU/857, G/SPS/N/EU/858, G/SPS/N/EU/863
Actualización
Panorama de las últimas autorizaciones de aditivos para piensos y su uso en nutrición animal en animales diana.
¿qué está cambiando?
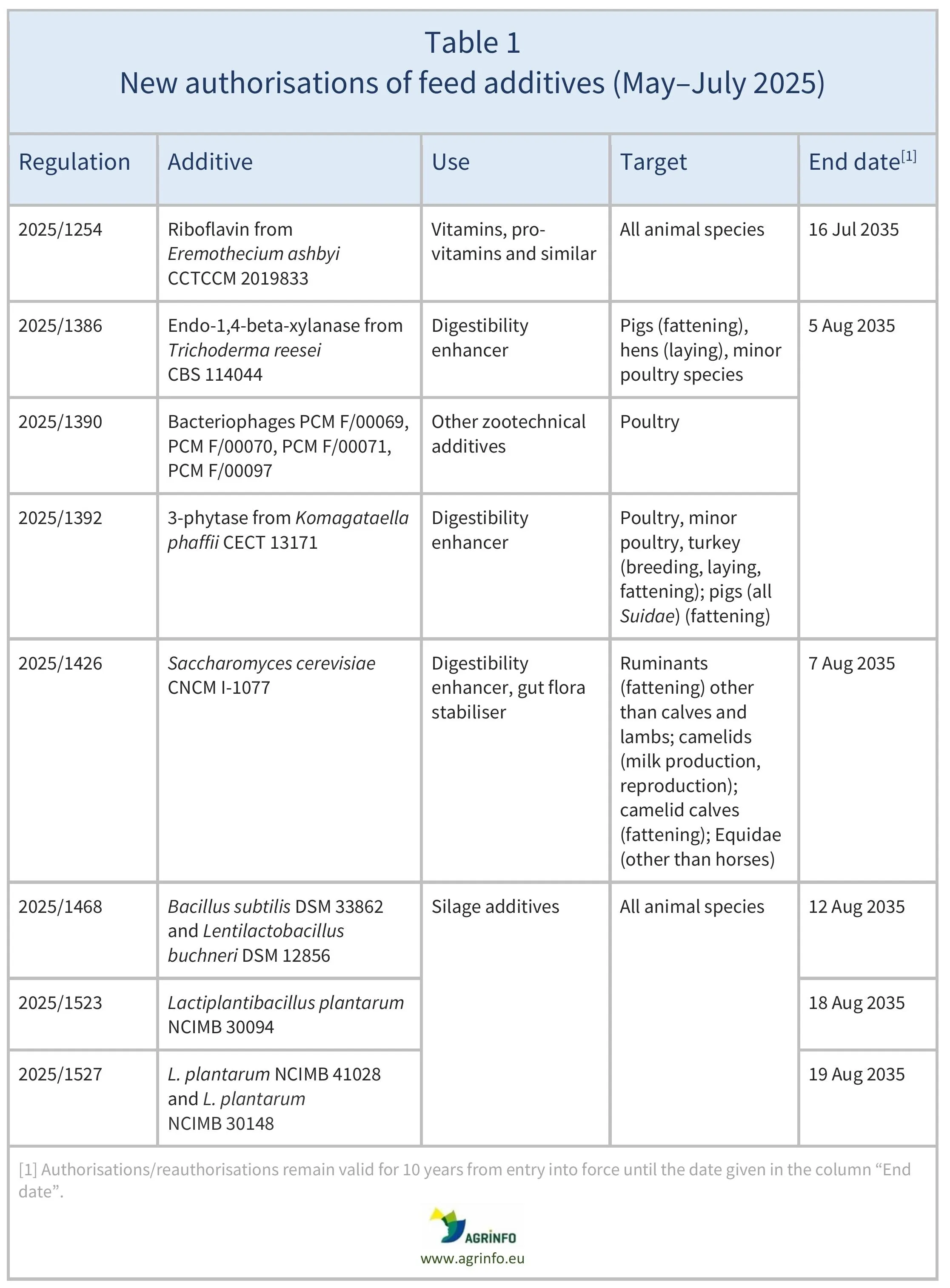
Autorizaciones
En mayo-julio de 2025, la Unión Europea (UE) autorizó los aditivos para piensos enumerados en el cuadro 1, basándose en los dictámenes publicados por la Autoridad Europea de Seguridad Alimentaria (EFSA; véase Recursos). Las condiciones de uso se describen en las regulaciones respectivas.
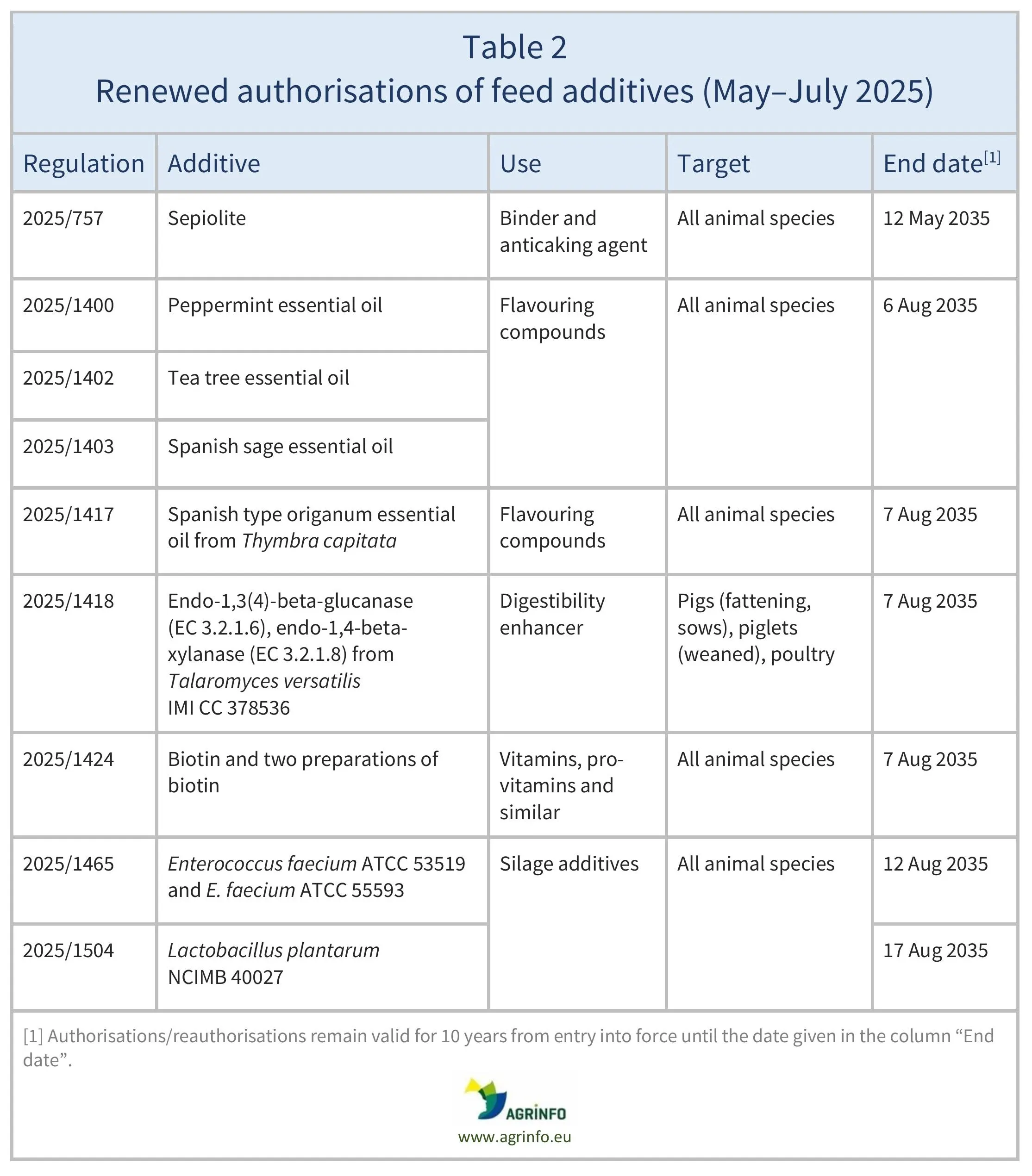
Reautorizaciones
En mayo-julio de 2025, la UE renovó las autorizaciones de los aditivos para piensos enumerados en el cuadro 2, basándose en los dictámenes publicados por la EFSA (véanse los Recursos). Las condiciones de uso se describen en las regulaciones respectivas.
La Comisión Europea ha informado al Comité de Medidas Sanitarias y Fitosanitarias (MSF) de la Organización Mundial del Comercio (OMC) de que tiene la intención de renovar la autorización de la tintura de eucalipto de Eucalyptus globulus como compuesto aromatizante en los piensos destinados a animales productores de alimentos enumerados en el proyecto de anexo de G/SPS/N/EU/857. También tiene la intención de renovar la autorización del aceite esencial de semillas de apio para los animales destinados a la producción de alimentos enumerados en el proyecto de anexo de G/SPS/N/EU/858.
Correcciones y modificaciones
- El Reglamento 2025/1391 corrige el Reglamento 2024/1186 relativo a la concentración de metileugenol en el aceite esencial de corteza de canela, que no debe superar el 0,004%.
- El Reglamento 2025/1395 modifica y corrige el Reglamento 2020/997 relativo al aditivo para piensos L-lisina base (líquida) producida con Corynebacterium glutamicum NRRL B-67439 o con C. glutamicum NRRL B-67535 para todas las especies animales (autorizado hasta el 30 de julio de 2030).
- El Reglamento 2025/1419 modifica los Reglamentos 2020/148, 2021/2094 y 2023/1172 en lo que respecta al cambio de nombre del titular de la autorización de los aditivos para piensos decoquinato (Deccox y Avi-Deccox 60G), clorhidrato de robenidina (Robenz 66G) y un preparado de lasalocid A de sodio (Avatec 150 G).
- El Reglamento 2025/1423 modifica el Reglamento 684/2014 en relación con el preparado de cantaxantina producida por fermentación con Yarrowia lipolytica CBS 146148 como aditivo en piensos para gallinas reproductoras.
- El Reglamento 2025/1426 modifica el Reglamento 2020/149 modificando la autorización de un preparado de Saccharomyces cerevisiae CNCM I-1077 como aditivo en piensos para corderos.
Retiradas
La Comisión Europea ha informado al Comité MSF de la OMC de su intención de retirar la tintura de eucalipto y el aceite esencial de semilla de apio como compuestos aromatizantes en los piensos para determinadas especies o categorías de animales. Asimismo, tiene la intención de retirar otros aditivos para piensos enumerados en el proyecto de anexo del documento G/SPS/N/EU/863, ya sea para todas las especies y categorías de animales (parte 1) o para especies y categorías específicas (parte 2).
En el caso de los aditivos para piensos autorizados anteriormente sin límite de tiempo, pero que ahora se retiran del mercado, se aplica un período transitorio.
¿Por qué?
Las solicitudes de las autorizaciones mencionadas fueron presentadas y examinadas por el laboratorio de referencia creado por el Reglamento sobre aditivos para piensos(1831/2003). Dicho Reglamento también exige que los aditivos para piensos se retiren del mercado si no se ha presentado ninguna solicitud antes del plazo previsto, o si se presentó una solicitud pero se retiró posteriormente. En los casos en que sólo se hayan presentado o retirado solicitudes para determinadas especies o categorías de animales, la retirada sólo afectará a las especies y categorías especificadas.
Cronología
Las autorizaciones siguen siendo válidas hasta las fechas finales que figuran en los cuadros 1 y 2.
Periodo transitorio para las retiradas
- existencias actuales, 12 meses
- premezclas, 15 meses
- piensos compuestos, 24 meses.
¿cuáles son las principales consecuencias para los países exportadores?
Con estas autorizaciones, habrá más aditivos para piensos disponibles en el mercado. Las autorizaciones y renovaciones tienen una validez de 10 años. El uso de todos los preparados y sustancias especificados como aditivos para piensos debe ajustarse a las disposiciones de uso especificadas en el anexo de cada reglamento.
Acciones recomendadas
Se recomienda a los países no pertenecientes a la UE que producen aditivos para piensos, piensos compuestos y materias primas para piensos destinados a la exportación a la UE que comprueben la situación de los aditivos en el registro de aditivos para piensos de la UE.
Para poder filtrar y ver más información, se aconseja descargar el registro en Excel (véase Portal de Información sobre Alimentos y Piensos: Aditivos para piensos > Descargar el registro en formato Excel).
Antecedentes
El procedimiento para autorizar la comercialización y el uso de aditivos para piensos se establece en el Reglamento 1831/2003.
Recursos
Registro deaditivos para piensos de la UE
Regulación 1831/2003 sobre aditivos para uso en nutrición animal
EFSA (2013a) Dictamen científico sobre la seguridad y eficacia de CAROPHYLL® Red 10% (preparado de cantaxantina) para todas las aves de corral destinadas a la reproducción (pollos, pavos y otras aves de corral). Revista de la EFSA, 11(1): 3047.
EFSA (2013b) Dictamen científico sobre la seguridad y eficacia de Enterococcus faecium (NCIMB 10415, DSM 22502, ATCC 53519 y ATCC 55593) como aditivos de ensilado para todas las especies animales. EFSA Journal, 11(10): 3363.
EFSA (2021a) Safety and efficacy of the feed additive consisting of Vitamin B2/Riboflavin produced by Eremothecium ashbyiCCTCCM2019833 for all animal species (Hubei Guangji Pharmaceutical Co., Ltd.). EFSA Journal, 19(3): 6462.
EFSA (2021b) Safety and efficacy of a feed additive consisting on the bacteriophages PCM F/00069, PCM F/00070, PCM F/00071 and PCM F/00097 infecting Salmonella Gallinarum B/00111 (Bafasal®) for all avian species (Proteon Pharmaceuticals S.A.). EFSA Journal, 19(5): e6534.
EFSA (2022a) Safety and efficacy of a feed additive consisting of sepiolite for all animal species (Sepiol S.A and Tolsa, S.A). EFSA Journal, 20(4): 7250.
EFSA (2022b) Assessment of the efficacy of two feed additives consisting of Enterococcus faecium ATCC 53519 and E. faecium ATCC 55593 for all animal species (FEFANA asbl). EFSA Journal, 20(10): e7603.
EFSA (2022c) Safety and efficacy of a feed additive consisting of 3-phytase produced by Komagataella phaffii (CECT 13171) (FSF10000/FLF1000) for poultry species, pigs for fattening and minor porcine species (FERTINAGRO BIOTECH S.L.). EFSA Journal, 20(11): e7614.
EFSA (2023a) Safety and efficacy of a feed additive consisting of the bacteriophages PCM F/00069, PCM F/00070, PCM F/00071 and PCM F/00097 (Bafasal®) for all avian species (Proteon Pharmaceuticals S.A.). EFSA Journal, 21(3): e7861
EFSA (2023b) Eficacia de los aditivos para piensos consistentes en Enterococcus faecium ATCC 53519 y E. faecium ATCC 55593 para todas las especies animales (FEFANA asbl). EFSA Journal, 21(7): e8166.
EFSA (2024a) Safety and efficacy of a feed additive consisting of an essential oil obtained from the fruit of Carum carvi L. (caraway oil) for all animal species (FEFANA asbl). EFSA Journal, 22(7): e8906.
EFSA (2024b) Safety and efficacy of a feed additive consisting of an essential oil obtained from the fruit of Apium graveolensL. (celery seed oil) for all animal species (FEFANA asbl). EFSA Journal, 22(7): e8907.
EFSA (2024c) Safety and efficacy of a feed additive consisting of a tincture derived from the leaves of Eucalyptus globulusLabill. (tintura de eucalipto) para todas las especies animales (FEFANA asbl). EFSA Journal, 22(5): e8801.
EFSA (2024d) Safety of a feed additive consisting of sepiolite for all animal species (Sepiol S.A. and Tolsa S.A.). EFSA Journal, 22(6): e8850.
EFSA (2024e) Modificación de los términos de autorización relativos al aditivo consistente en L-lisina base líquida producida con Corynebacterium glutamicum NRRL B-67439 y NRRL B-67535 para todas las especies animales (ADM specialty ingredients (Europe) B.V.). EFSA Journal, 22(7): e8950.
EFSA (2024f) Safety and efficacy of a feed additive consisting of an essential oil derived from the leaves of Salvia officinalis ssp. lavandulifolia (Vahl) Gams (Spanish sage oil) for use in all animal species (FEFANA asbl). EFSA Journal, 22(10): e9015.
EFSA (2024g) Safety and efficacy of a feed additive consisting of an essential oil derived from the flowering stems of Salvia sclarea L. (clary sage oil) for use in all animal species (FEFANA asbl). EFSA Journal, 22(11): e9016.
EFSA (2024h) Safety and efficacy of a feed additive consisting of Bacillus subtilis DSM 33862 and Lentilactobacillus buchneri DSM 12856 as a silage additive for all animal species (Lactosan GmbH & Co.KG). EFSA Journal, 22(11): e9070.
EFSA (2024i) Safety and efficacy of a feed additive consisting of an essential oil derived from the flowering tops of Lavandula angustifolia Mill. (aceite de lavanda) para su uso en todas las especies animales (FEFANA asbl). EFSA Journal, 22(11): e9017.
EFSA (2024j) Safety and efficacy of a feed additive consisting of an essential oil derived from the flowering tops of Thymbra capitata (L.) Cav. (Spanish type origanum oil) for use in all animal species (FEFANA asbl). EFSA Journal, 22(10): e9018.
EFSA (2024k) Safety of a feed additive consisting of 3-phytase produced with Komagataella phaffii CECT 13171 (FSF10000/FLF1000) for poultry species, pigs for fattening and minor porcine species for fattening (Fertinagro Biotech S.L.). EFSA Journal, 22(10): e9023.
EFSA (2024l) Safety and efficacy of a feed additive consisting of endo-1,4-β-xylanase produced with Trichoderma reesei CBS 114044 (ECONASE® XT) for pigs for fattening, laying hens and minor poultry species (AB Enzymes Finland Oy). EFSA Journal, 22(10): e9025.
EFSA (2024m) Safety and efficacy of a feed additive consisting of an essential oil derived from leaves and terminal branchlets of Melaleuca alternifolia (Maiden & Betche) Cheel (tea tree oil) for use in all animal species (FEFANA asbl). EFSA Journal, 22(10): e9026.
EFSA (2024n) Safety of a feed additive consisting of vitamin B2/riboflavin produced with Eremothecium ashbyi CCTCCM 2019833 for all animal species (Hubei Guangji Pharmaceutical Co., Ltd). EFSA Journal, 22(11): e9073.
EFSA (2024o) Assessment of the modification of the authorisation of the feed additive consisting of Saccharomyces cerevisiaeCNCMI-1077 for lambs and its extension of use to all ruminants and camelids reared for milk production/suckling/reproduction, all minor (young) ruminant species and camelids for fattening and Equidae other than horses (Lallemand SAS). EFSA Journal, 22(11): e9075.
EFSA (2024p) Safety and efficacy of a feed additive consisting of the bacteriophages PCM F/00069, PCM F/00070, PCM F/00071 and PCM F/00097 (Bafasal®) for all poultry (Proteon Pharmaceuticals S.A.). EFSA Journal, 22(12): e9132.
EFSA (2024q) Assessment of the feed additive consisting of Lactiplantibacillus plantarum NCIMB 40027 for all animal species for the renewal of its authorisation (Volac International ltd). EFSA Journal, 22(12): e9145.
EFSA (2024r) Safety and efficacy of a feed additive consisting of an essential oil derived from the leaves of Salvia officinalis L. (sage oil) for use in all animal species (FEFANA asbl). EFSA Journal, 22(12): e9135.
EFSA (2024s) Safety and efficacy of a feed additive consisting of Lactiplantibacillus plantarum NCIMB 41028 for all animal species (Genus Breeding Ltd.). EFSA Journal, 22(12): e9142.
EFSA (2024t) Safety and efficacy of a feed additive consisting of Lactiplantibacillus plantarum NCIMB 30148 for all animal species (Genus Breeding Ltd.). EFSA Journal, 22(12): e9143.
EFSA (2024u) Efficacy of the feed additives consisting of Enterococcus faecium ATCC 53519 and E. faecium ATCC 55593 as silage additives for all animal species (FEFANA asbl). EFSA Journal, 22(11): e9071.
EFSA (2025a) Safety and efficacy of a feed additive consisting of an essential oil derived from the aerial parts of Mentha×piperita L. (peppermint oil) for use in all animal species (FEFANA asbl). EFSA Journal, 23(1): e9076.
EFSA (2025b) Safety and efficacy of a feed additive consisting of Lactiplantibacillus plantarum NCIMB 30094 for all animal species (Volac International Ltd). EFSA Journal, 23(1): e9144.
EFSA (2025c) Modificación de los términos de autorización del aditivo para piensos consistente en un preparado de cantaxantina (CAROPHYLL® Red 10%) para gallinas reproductoras a fin de incluir cantaxantina producida con Yarrowia lipolytica CBS 146148 (DSM Nutritional Products Ltd). EFSA Journal, 23(1): e9133.
EFSA (2025d) Assessment of the feed additive consisting of biotin for all animal species for the renewal of its authorisation (ADISSEO, DSM Nutritional Products Ltd., NHU Europe GmbH). EFSA Journal, 23(2): e9250.
EFSA (2025e) Assessment of the feed additive consisting of endo-1,3(4)-beta-glucanase and endo-1,4-beta-xylanase (produced with Talaromyces versatilis IMI CC 378536) (Rovabio® Excel) for all poultry species, weaned piglets, pigs for fattening and sows for the renewal of its authorisation (Adisseo France SAS). EFSA Journal, 23(1): e9131.
Fuentes
Reglamentos de aplicación de la Comisión 2025/757, 2025/1254, 2025/1386, 2025/1390, 2025/1391, 2025/1392, 2025/1395, 2025/1400, 2025/1402, 2025/1403, 2025/1417, 2025/1418, 2025/1419, 2025/1423, 2025/1424, 2025/1426, 2025/1465, 2025/1468, 2025/1504, 2025/1523, 2025/1527
Notificaciones G/SPS/N/EU/857, G/SPS/N/EU/858, G/SPS/N/EU/863
Descargo de responsabilidad: COLEAD no se hace responsable de ninguna pérdida, daño, responsabilidad o gasto incurrido o sufrido como resultado de la utilización de la información disponible en este sitio web o de cualquier enlace a sitios externos. El uso del sitio web es por cuenta y riesgo exclusivo del usuario. Esta plataforma de información ha sido elaborada y mantenida con el apoyo financiero de la Unión Europea. No obstante, su contenido no refleja las opiniones de la Unión Europea.
La UE autoriza determinados aditivos para piensos y retira otros
Commission Implementing Regulations 2025/757, 2025/1254, 2025/1386, 2025/1390, 2025/1391, 2025/1392, 2025/1395, 2025/1400, 2025/1402, 2025/1403, 2025/1417, 2025/1418, 2025/1419, 2025/1423, 2025/1424, 2025/1426, 2025/1465, 2025/1468, 2025/1504, 2025/1523, 2025/1527
Notifications G/SPS/N/EU/857, G/SPS/N/EU/858, G/SPS/N/EU/863
¿qué está cambiando y por qué?
Autorizaciones y reautorizaciones
Entre mayo y julio de 2025, la Unión Europea (UE) autorizó los aditivos para piensos enumerados en el cuadro 1, y renovó las autorizaciones de los aditivos para piensos enumerados en el cuadro 2. Estas autorizaciones se basan en dictámenes publicados por la Autoridad Europea de Seguridad Alimentaria (EFSA). Las condiciones de uso se describen en las regulaciones respectivas.
La UE también ha informado al Comité de Medidas Sanitarias y Fitosanitarias (MSF) de la Organización Mundial del Comercio (OMC) de su intención de renovar las autorizaciones de la tintura de eucalipto y del aceite esencial de semilla de apio como compuestos aromatizantes en los piensos para determinados animales destinados a la producción de alimentos, y de retirar las autorizaciones para su uso en piensos para otros animales.
Retiradas
La UE también ha notificado al Comité MSF de la OMC su intención de retirar otros aditivos para piensos. Los aditivos para piensos se retiran del mercado si no se ha presentado ninguna solicitud de renovación antes del plazo previsto, o si se presentó una solicitud pero posteriormente se retiró. En el caso de estos aditivos para piensos, se aplica un periodo transitorio durante el cual pueden agotarse las existencias restantes. En los casos en que sólo se hayan presentado o retirado solicitudes para determinadas especies o categorías de animales, la retirada sólo afecta a las especies y categorías especificadas.
Acciones
Se recomienda a los países no pertenecientes a la UE que producen aditivos para piensos, piensos compuestos y materias primas para piensos destinados a la exportación a la UE que comprueben la situación de los aditivos en el registro de aditivos para piensos de la UE.
Para poder filtrar y ver más información, se aconseja descargar el registro en Excel (véase Portal de Información sobre Alimentos y Piensos: Aditivos para piensos > Descargar el registro en formato Excel).
Cronología
Las autorizaciones siguen siendo válidas hasta las fechas finales que figuran en los cuadros 1 y 2.
Periodo transitorio para las retiradas
- existencias actuales, 12 meses
- premezclas, 15 meses
- piensos compuestos, 24 meses.
Tablas y figuras
Descargo de responsabilidad: COLEAD no se hace responsable de ninguna pérdida, daño, responsabilidad o gasto incurrido o sufrido como resultado de la utilización de la información disponible en este sitio web o de cualquier enlace a sitios externos. El uso del sitio web es por cuenta y riesgo exclusivo del usuario. Esta plataforma de información ha sido elaborada y mantenida con el apoyo financiero de la Unión Europea. No obstante, su contenido no refleja las opiniones de la Unión Europea.