Aditivos para piensos: Noviembre/diciembre de 2024 autorizaciones, reautorizaciones y usos previstos
- Feed additives
- Feed safety
Resumen
Una visión general de las últimas autorizaciones y reautorizaciones de aditivos para piensos, y actualizaciones de la lista de usos previstos en la alimentación animal para animales diana.
La UE autoriza o reautoriza determinados aditivos para piensos y actualiza la lista de usos previstos - noviembre/diciembre de 2024
Reglamentos de aplicación de la Comisión 2024/2899, 2024/3162, 2024/3166, 2024/3167, 2024/3168
Actualización
Una visión general de las últimas autorizaciones y reautorizaciones de aditivos para piensos, y actualizaciones de la lista de usos previstos en la alimentación animal para animales diana.
Productos afectados
Aditivos para piensos
¿qué está cambiando?
Autorizaciones y reautorizaciones
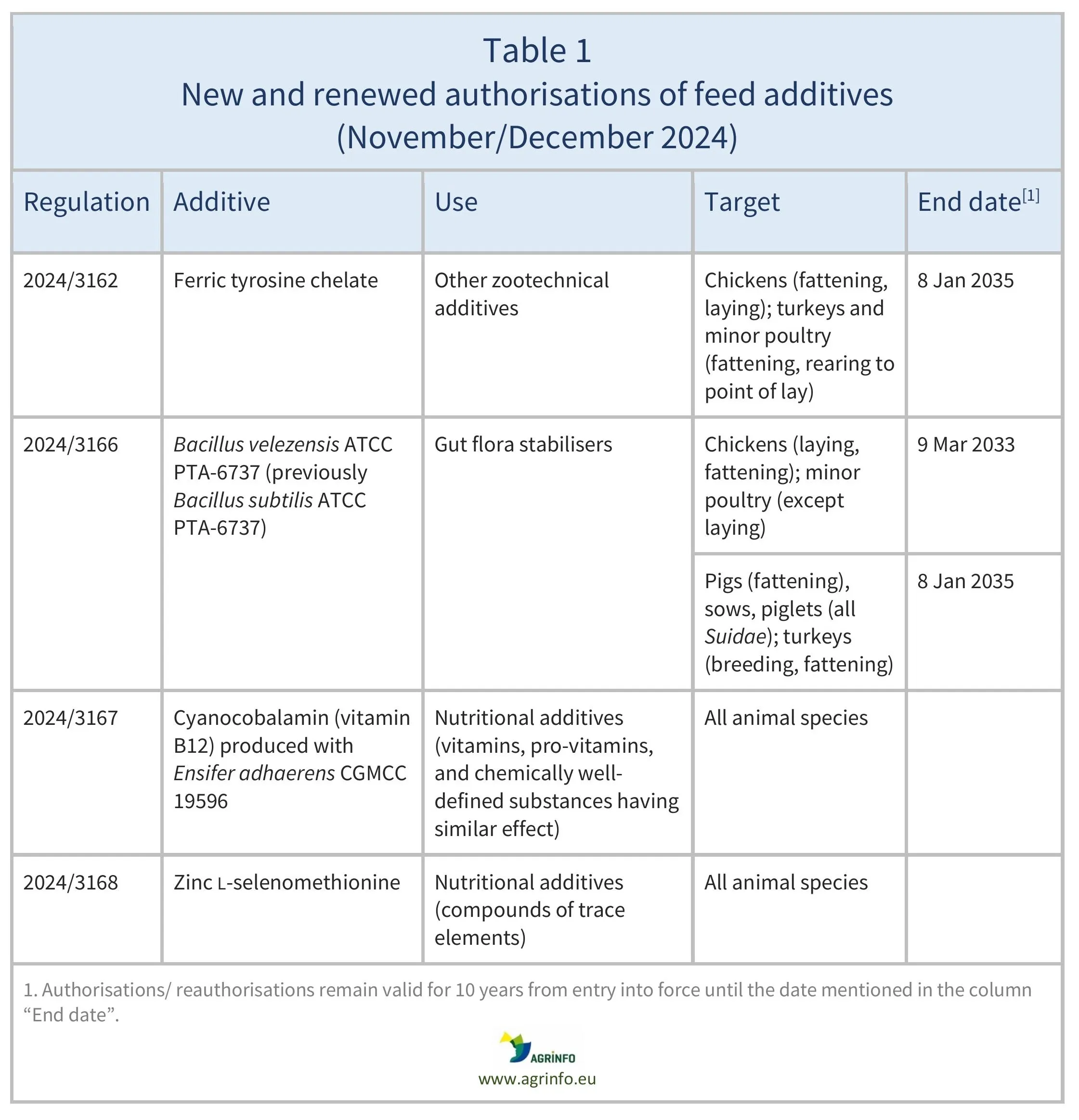
En noviembre y diciembre de 2024, la UE autorizó y reautorizó los aditivos para piensos enumerados en el cuadro 1. Estas autorizaciones y reautorizaciones se basan en dictámenes publicados por la Autoridad Europea de Seguridad Alimentaria (EFSA 2019, 2023a, 2023b, 2024a, 2024b). Las condiciones de uso se describen en las regulaciones respectivas.
Actualizaciones de la lista de usos previstos
El uso de 1,25-dihidroxicolecalciferol glicosilado de extracto de Solanum glaucophyllum para reducir el riesgo de fiebre puerperal e hipocalcemia subclínica (niveles bajos de calcio) en vacas se incluye ahora en la lista de usos previstos de los piensos destinados a objetivos de nutrición específicos (Reglamento 2024/2899).
¿Por qué?
Las solicitudes de estas autorizaciones y reautorizaciones fueron examinadas por el Laboratorio de Referencia creado por el Reglamento sobre aditivos para piensos(1831/2003).
La EFSA (2022) concluyó que el 1,25-dihidroxicolecalciferol glicosilado del extracto de S. glaucophyllum, administrado por vía oral en un pienso complementario desde 9 días antes del parto hasta inmediatamente antes del parto, tiene potencial para prevenir la hipocalcemia en vacas lecheras.
Cronología
Las autorizaciones y reautorizaciones siguen siendo válidas hasta las fechas finales que figuran en el cuadro 1.
¿cuáles son las principales consecuencias para los países exportadores?
Con estas autorizaciones, habrá más aditivos para piensos disponibles en el mercado. Las autorizaciones y renovaciones tienen una validez de 10 años. Todos los aditivos para piensos deben utilizarse tal como se especifica en el anexo de cada regulación.
Acciones recomendadas
Se recomienda a los países no pertenecientes a la UE que producen aditivos para piensos, piensos compuestos y materias primas para piensos destinados a la exportación a la UE que comprueben su situación en el registro de aditivos para piens os de la UE.
Para poder filtrar y ver más información, puede descargar el registro en formato Excel (véase la página web del Portal de Información sobre Alimentos y Piensos > Aditivos para piensos > Descargar el registro en formato Excel).
Antecedentes
El procedimiento para autorizar la comercialización y el uso de aditivos para piensos se establece en el Reglamento 1831/2003. Para conocer las últimas actualizaciones sobre aditivos para piensos, consulte el registro de aditivos para piensos de la UE.
Recursos
Comisión Europea: Base de datos del portal de información sobre alimentos y piensos: Aditivos para piensos
Reglamento 1831/2003 sobre los aditivos en la alimentación animal
EFSA (2024a) Assessment of the feed additive consisting of Bacillus velezensis ATCC PTA-6737 (PB6) for turkeys for fattening and turkeys reared for breeding for the renewal of its authorisation and the modification of the conditions of the authorisation for other growing poultry species (Kemin Europe N.V). EFSA Journal, 22: e8650.
EFSA (2024b) Safety and efficacy of a feed additive consisting of Bacillus velezensis ATCC PTA-6737 (PB6) for the renewal of the authorisations in weaned piglets, weaned minor porcine species and sows and the extension of use to all Suidae (Kemin Europe N.V). EFSA Journal, 22: e8562
EFSA (2023a) Modificación de los términos de la autorización de zinc-L-selenometionina como aditivo en piensos para todas las especies animales (Zinpro Animal Nutrition (Europe), Inc.). EFSA Journal, 21: e8459
EFSA (2023b) Safety and efficacy of a feed additive consisting of vitamin B12 (cyanocobalamin) produced by fermentation with Ensifer adhaerens CGMCC 19596 for all animal species (Hebei Huarong Pharmaceutical Co. ltd). EFSA Journal, 21(4): 7972.
EFSA (2022) Safety and efficacy of a feed additive consisting of Solanum glaucophyllum leaf extract for dairy cows and other dairy ruminants (Herbonis Animal Health Gmbh). EFSA Journal, 20(8): 7434.
EFSA (2019) Seguridad y eficacia de TYFER™ (quelato férrico de tirosina) como aditivo zootécnico para piensos destinados a pollos, pavos y especies menores de aves de corral de engorde o criadas para puesta/recría. Revista de la EFSA, 17(2): 5608.
Fuentes
Reglamento de aplicación de la Comisión:
2024/2899 por el que se establece una lista de usos previstos de los piensos destinados a objetivos de nutrición específicos
2024/3162 relativo a la autorización del quelato de tirosina férrica como aditivo en piensos para todas las especies de aves de corral de engorde, todas las especies de aves de corral de puesta, y pavos y especies menores de aves de corral de cría (titular de la autorización: Akeso Biomedical, Inc. EE.UU., representada en la Unión por Pen & Tec Consulting SLU)
2024/3166 relativa a la renovación de la autorización de un preparado de Bacillus velezensis ATCC PTA-6737 como aditivo en piensos para pavos de engorde, pavos criados para reproducción, lechones destetados, suidos destetados distintos del Sus scrofa domesticus y cerdas, su autorización para cerdos de engorde de todas las especies de suidos, lechones lactantes de todas las especies de suidos y cerdas de especies menores de suidos (titular de la autorización: Kemin Europa N.V.)
2024/3167 relativa a la autorización de cianocobalamina (vitamina B12) producida con Ensifer adhaerens CGMCC 19596 como aditivo para piensos destinados a todas las especies animales
2024/3168 relativo a la autorización de un preparado de zinc-L-selenometionina como aditivo en piensos para todas las especies animales
Descargo de responsabilidad: COLEAD no se hace responsable de ninguna pérdida, daño, responsabilidad o gasto incurrido o sufrido como resultado de la utilización de la información disponible en este sitio web o de cualquier enlace a sitios externos. El uso del sitio web es por cuenta y riesgo exclusivo del usuario. Esta plataforma de información ha sido elaborada y mantenida con el apoyo financiero de la Unión Europea. No obstante, su contenido no refleja las opiniones de la Unión Europea.
La UE autoriza o reautoriza determinados aditivos para piensos y actualiza la lista de usos previstos - noviembre/diciembre de 2024
Commission Implementing Regulations 2024/2899, 2024/3162, 2024/3166, 2024/3167, 2024/3168
¿qué está cambiando y por qué?
En noviembre y diciembre de 2024, la UE autorizó o volvió a autorizar los aditivos para piensos que figuran en el cuadro 1. Estas decisiones se basan en dictámenes publicados por la Autoridad Europea de Seguridad Alimentaria (EFSA). Todos los aditivos para piensos deben utilizarse tal como se especifica en el anexo de cada regulación.
La EFSA validó el uso del extracto de Solanum glaucophyllum para reducir el riesgo de fiebre puerperal y de hipocalcemia subclínica (niveles bajos de calcio) en las vacas antes del parto, y ahora se incluye en la lista de usos previstos de los piensos destinados a objetivos de nutrición específicos.
Acciones
Se recomienda a los países no pertenecientes a la UE que producen aditivos para piensos, piensos compuestos y materias primas para piensos destinados a la exportación a la UE que comprueben su situación en el registro de aditivos para piens os de la UE.
Para poder filtrar y ver más información, puede descargar el registro en formato Excel (véase la página web del Portal de Información sobre Alimentos y Piensos > Aditivos para piensos > Descargar el registro en formato Excel).
Cronología
Las autorizaciones y reautorizaciones siguen siendo válidas hasta las fechas finales que figuran en el cuadro 1.
Tablas y figuras
Descargo de responsabilidad: COLEAD no se hace responsable de ninguna pérdida, daño, responsabilidad o gasto incurrido o sufrido como resultado de la utilización de la información disponible en este sitio web o de cualquier enlace a sitios externos. El uso del sitio web es por cuenta y riesgo exclusivo del usuario. Esta plataforma de información ha sido elaborada y mantenida con el apoyo financiero de la Unión Europea. No obstante, su contenido no refleja las opiniones de la Unión Europea.