Nuevo alimento: oleorresina de algas rica en astaxantina
- Food safety
- Novel/traditional foods
- Food information
- Labelling
Resumen
La Comisión Europea ha aprobado un cambio en las especificaciones del nuevo alimento oleorresina rica en astaxantina procedente del alga Haematococcus pluvialis.
La UE aprueba un cambio en las especificaciones de la oleorresina rica en astaxantina del alga Haematococcus pluvialis
Reglamento de Ejecución (UE) 2024/1026 de la Comisión, de 8 de abril de 2024, por el que se modifica el Reglamento de Ejecución (UE) 2017/2470 en lo que respecta a las especificaciones de la nueva oleorresina alimentaria rica en astaxantina procedente del alga Haematococcus pluvialis
Actualización
La Comisión Europea ha aprobado un cambio en las especificaciones del nuevo alimento oleorresina rica en astaxantina procedente del alga Haematococcus pluvialis.
¿qué está cambiando?
El presente Reglamento autoriza la reducción de los límites mínimos de especificación para los monoésteres de proteína y astaxantina (ATX), y el aumento de los límites máximos de especificación para las cantidades relativas de diésteres de ATX y estereoisómeros 9-cis en el total de ATX (véase el cuadro 1).
¿Por qué?
La EFSA(2023) concluyó que los cambios propuestos en las especificaciones son seguros en la ingesta diaria admisible (IDA) de ATX procedente de complementos alimenticios en 0,2 mg/kg de peso corporal.
Cronología
Las nuevas especificaciones se aplicarán a partir del 29 de abril de 2024.
Acciones recomendadas
Los exportadores de complementos alimenticios que contengan esta sustancia deben garantizar que se respetan las nuevas especificaciones establecidas en el cuadro 1.
Antecedentes
La astaxantina es un carotenoide producido a partir del alga H. pluvialis, cuyo uso en complementos alimenticios para la población general se autorizó por primera vez mediante el Reglamento (UE) 2017/2470.
El Reglamento de Ejecución (UE ) 2021/1377 limitó sus condiciones de uso a adultos y adolescentes mayores de 14 años basándose en un dictamen de la EFSA (2020).
El Reglamento de Ejecución (UE) 2023/1581 autorizó su uso en complementos alimenticios destinados a niños de 3 a 10 años y adolescentes de 10 a 14 años, siempre que la ingesta de ATX procedente de complementos alimenticios no superara una IDA de 0,2 mg/kg de peso corporal al día.
Para más información sobre el proceso de autorización de nuevos alimentos, véase Explicación de los nuevos alimentos.
Recursos
EFSA (2023) Seguridad de un cambio en las especificaciones de la nueva oleorresina alimentaria de Haematococcus pluvialis que contiene astaxantina de conformidad con el Reglamento (UE) 2015/2283. EFSA Journal, 21(11): 5993.
EFSA (2020) Seguridad de la astaxantina para su uso como nuevo alimento en complementos alimenticios. EFSA Journal, 18(2): 8338.
Reglamento de Ejecución (UE) 2017/2470 por el que se establece la lista de nuevos alimentos
Reglamento de Ejecución (UE) 2021/1377 por el que se autoriza la modificación de las condiciones de uso del nuevo alimento oleorresina rica en astaxantina del alga Haematococcus pluvialis
Reglamento de Ejecución (UE) 2023/1581 por lo que se refiere a las condiciones de uso del nuevo alimento "oleorresina rica en astaxantina de alga Haematococcus pluvialis "
Fuentes
Reglamento de Ejecución (UE) 2024/1026 en lo que respecta a las especificaciones de la nueva oleorresina alimentaria rica en astaxantina procedente del alga Haematococcus pluvialis
Tablas y figuras
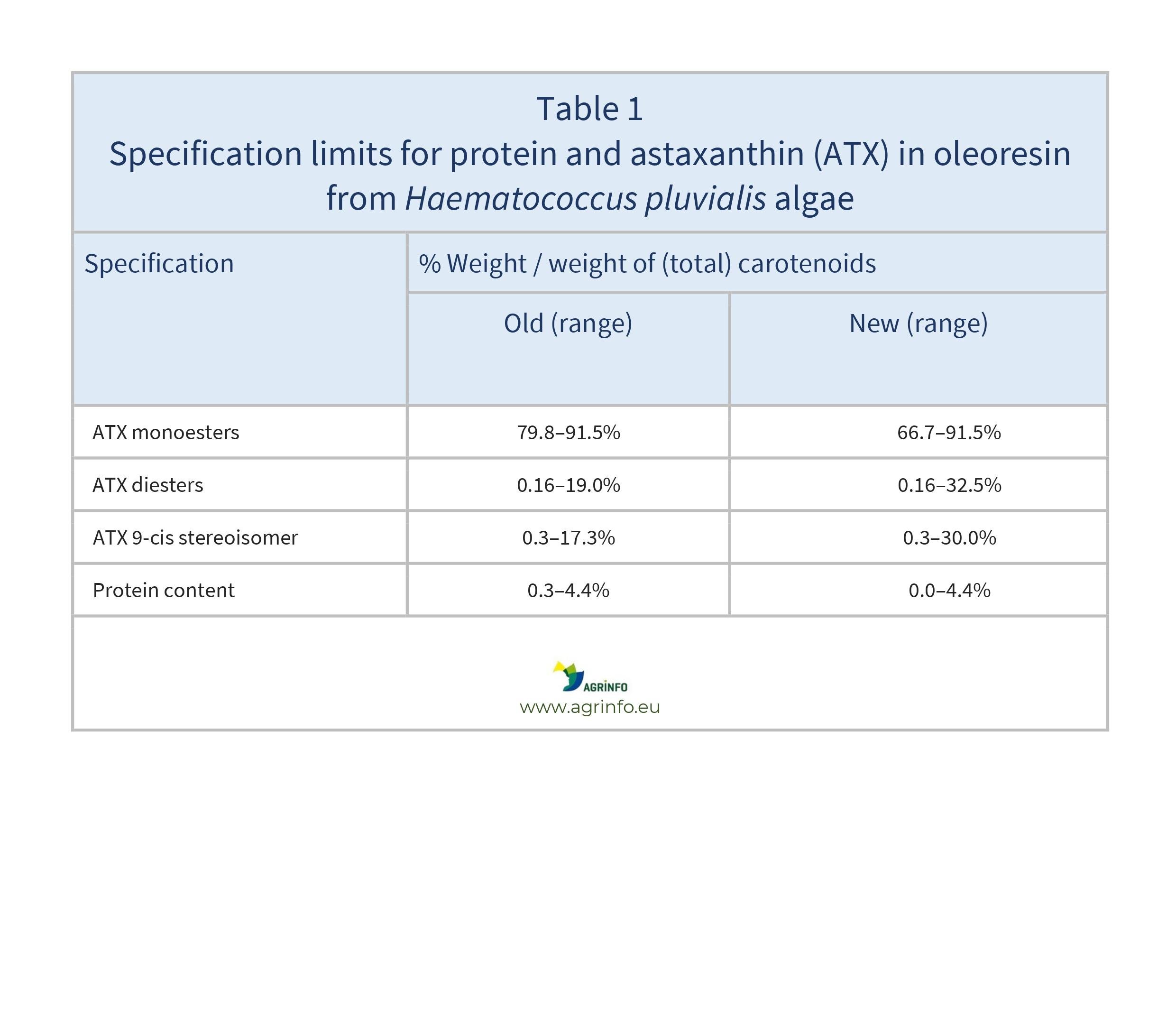
Source: Implementing Regulation (EU) 2024/1026
Descargo de responsabilidad: COLEAD no se hace responsable de ninguna pérdida, daño, responsabilidad o gasto incurrido o sufrido como resultado de la utilización de la información disponible en este sitio web o de cualquier enlace a sitios externos. El uso del sitio web es por cuenta y riesgo exclusivo del usuario. Esta plataforma de información ha sido elaborada y mantenida con el apoyo financiero de la Unión Europea. No obstante, su contenido no refleja las opiniones de la Unión Europea.
La UE aprueba un cambio en las especificaciones de la oleorresina rica en astaxantina del alga Haematococcus pluvialis
Regulation 2024/1026 as regards the specifications of the novel food astaxanthin-rich oleoresin from Haematococcus pluvialis algae
¿qué está cambiando y por qué?
La Comisión Europea ha aprobado un cambio en las especificaciones del nuevo alimento oleorresina rica en astaxantina procedente del alga Haematococcus pluvialis. Los complementos alimenticios que contienen astaxantina (ATX), un carotenoide, están autorizados para adultos, niños de 3 a 10 años y adolescentes de 10 a 14 años. La Autoridad Europea de Seguridad Alimentaria (EFSA) concluyó que su uso es seguro siempre que la ingesta de ATX no supere la ingesta diaria admisible (IDA) de 0,2 mg/kg de peso corporal al día. El presente Reglamento autoriza límites mínimos más bajos para las proteínas y los monoésteres de ATX, y límites máximos más elevados para los diésteres de ATX y el estereoisómero 9-cis en el total de ATX (véase el cuadro 1).
Acciones
Los exportadores de complementos alimenticios que contengan esta sustancia deben garantizar que se respetan las nuevas especificaciones establecidas en el cuadro 1.
Cronología
Las nuevas especificaciones se aplicarán a partir del 29 de abril de 2024.
Tablas y figuras

Source: Implementing Regulation (EU) 2024/1026
Descargo de responsabilidad: COLEAD no se hace responsable de ninguna pérdida, daño, responsabilidad o gasto incurrido o sufrido como resultado de la utilización de la información disponible en este sitio web o de cualquier enlace a sitios externos. El uso del sitio web es por cuenta y riesgo exclusivo del usuario. Esta plataforma de información ha sido elaborada y mantenida con el apoyo financiero de la Unión Europea. No obstante, su contenido no refleja las opiniones de la Unión Europea.
