Certificats sanitaires officiels : chevaux producteurs de denrées alimentaires et produits équins
- Animal health
- Animal health certification
- Food safety
- Third country lists
- Veterinary residues
- Animal health controls
- Food safety controls
- Official controls
Résumé
La Commission européenne a informé le Comité des mesures sanitaires et phytosanitaires (SPS) de l'Organisation mondiale du commerce(OMC) (G/SPS/N/EU/891) de son intention de modifier les certificats officiels requis pour exporter vers l'Union européenne (UE) des chevaux destinés à être utilisés dans l'alimentation et des produits dérivés du cheval. Les certificats doivent être modifiés pour refléter avec précision l'interdiction par l'UE de l'utilisation de certaines substances, telles que les substances thyréostatiques (antithyroïdiennes) et les stilbènes, qui doit s'appliquer non seulement au pays tiers exportateur, mais aussi au pays tiers où le cheval est né et a été élevé (si ce n'est pas le même).
L'UE va proposer des certificats sanitaires officiels révisés pour les chevaux producteurs de denrées alimentaires et les produits équins
Projet de règlement d'exécution de la Commission modifiant l'annexe III du règlement d'exécution (UE) 2020/2235 et l'annexe II du règlement d'exécution (UE) 2021/403 en ce qui concerne les modèles de certificat pour l'introduction dans l'Union de lots de certains produits d'origine domestique solipèdes destinés à la consommation humaine et à certaines catégories d'équidés
Mise à jour
La Commission européenne a informé le Comité des mesures sanitaires et phytosanitaires (SPS) de l'Organisation mondiale du commerce(OMC) (G/SPS/N/EU/891) de son intention de modifier les certificats officiels requis pour exporter vers l'Union européenne (UE) des chevaux destinés à être utilisés dans l'alimentation et des produits dérivés du cheval. Les certificats doivent être modifiés pour refléter avec précision l'interdiction par l'UE de l'utilisation de certaines substances, telles que les substances thyréostatiques (antithyroïdiennes) et les stilbènes, qui doit s'appliquer non seulement au pays tiers exportateur, mais aussi au pays tiers où le cheval est né et a été élevé (si ce n'est pas le même).
Produits concernés
Chevaux destinés à être utilisés dans les aliments et les produits pour chevaux
qu'est-ce qui change ?
L'Union européenne propose de modifier les certificats officiels requis pour l'exportation vers l'Union européenne de chevaux destinés à être utilisés dans les denrées alimentaires et les produits dérivés du cheval. Ces modifications concernent les modèles de certificats suivants : EQU, MP-PREP, MPNT, MPST :
Les détails des changements apportés à ces modèles de certificats sont donnés dans le tableau 1.
pourquoi ?
L'UE interdit l'utilisation de certaines substances, telles que les substances thyréostatiques (antithyroïdiennes) et les stilbènes, au cours de la vie d'un cheval si la viande de ce cheval est destinée à être consommée comme aliment dans l'UE (directive 96/22/CE). Les pays tiers impliqués dans la production de viande de cheval doivent être répertoriés dans le règlement 2021/405, annexe I (voir Listes de pays tiers pour la santé publique - expliquées).
Actuellement, le libellé des certificats officiels qui doivent accompagner les lots de ces produits ne reflète ces exigences que pour le pays exportateur. Il ne couvre pas le pays tiers où le cheval est né et a été élevé, s'il est différent du pays exportateur. Ce projet de règlement vise à aligner le libellé des certificats sur les exigences de la directive 96/22/CE, art. 3 (a), et Art. 11.
Calendrier
Les certificats modifiés devraient s'appliquer à partir du 30 octobre 2026.
Actions recommandées
Lorsqu'un pays tiers exporte des chevaux ou leurs produits originaires d'un autre pays tiers, le vétérinaire officiel qui signe le certificat d'exportation doit vérifier que ce pays tiers supplémentaire respecte pleinement les règles de l'UE (y compris la non-utilisation de substances interdites) et qu'il figure avec un "X" pour "équins" à l'annexe I du règlement (CE) n° 2021/405.
La consultation de l'OMC a été clôturée le 30 décembre 2025.
Contexte
La directive 96/22/CE du Conseil interdit l'utilisation des substances suivantes chez les chevaux producteurs de denrées alimentaires [article 3 (a)] et interdit l'importation dans l'UE de chevaux (et de leurs produits) auxquels ces substances ont été administrées (article 11) :
- Aristolochia spp. et préparations, chloramphénicol, chlorpromazine, colchicine, dapsone, dimétridazole, métronidazole, nitrofuranes, ronidazole (substances énumérées dans le règlement 37/2010, annexe, tableau 2)
- substances thyréostatiques, stilbènes, dérivés de stilbènes, leurs sels et esters, œstradiol 17β et ses dérivés estérifiés (directive 96/22/CE, annexe II).
D'autres substances ayant une action sur les hormones (action œstrogène, androgène ou gestagène) et les bêta-agonistes (utilisés pour augmenter la masse musculaire) sont également interdits, sauf s'ils sont nécessaires à des traitements thérapeutiques et/ou à l'élevage (directive 96/22/CE, annexe III).
Les produits dérivés du cheval ne peuvent être importés que des pays figurant à l'annexe I du règlement 2021/405 avec un "X" pour "équins", y compris le pays tiers où le cheval est né et a été élevé, s'il est différent du pays exportateur. Les pays qui autorisent l'utilisation des substances susmentionnées dans leur législation ne peuvent pas figurer dans cette annexe (directive 96/22/CE, article 11).
Les règles établissant les contrôles des résidus de substances pharmacologiquement actives ont été révisées en 2022 (voir Contrôles officiels des résidus de médicaments vétérinaires dans les produits d'origine animale et Contrôles officiels de l'utilisation des substances pharmacologiquement actives et de leurs résidus).
Pour une vue d'ensemble des certificats officiels, voir Certificats sanitaires officiels de l'UE pour les exportations vers l'UE - expliqué.
Ressources
Directive 96/22/CE du Conseil concernant l'interdiction d'utilisation de certaines substances à effet hormonal ou thyréostatique et des substances ß-agonistes dans les spéculations animales
Règlement délégué (UE) 2022/1644 de la Commission relatif aux exigences spécifiques pour la réalisation des contrôles officiels concernant l'utilisation des substances pharmacologiquement actives autorisées en tant que médicaments vétérinaires ou additifs pour l'alimentation animale, ainsi que des substances pharmacologiquement actives interdites ou non autorisées et de leurs résidus
Règlement d'exécution (UE) 2022/1646 de la Commission relatif aux modalités pratiques uniformes pour l'exécution des contrôles officiels concernant l'utilisation des substances pharmacologiquement actives autorisées en tant que médicaments vétérinaires ou additifs pour l'alimentation animale, ainsi que des substances pharmacologiquement actives interdites ou non autorisées et de leurs résidus, ainsi qu'au contenu spécifique des plans de contrôle nationaux pluriannuels et aux modalités particulières de leur élaboration
Commission européenne (2025) Lignes directrices concernant les conditions d'entrée dans l'UE des animaux et des produits d'origine animale - Plans de contrôle des résidus de médicaments vétérinaires, de pesticides et de contaminants
Sources
Projet de règlement d'exécution de la Commission en ce qui concerne les modèles de certificats pour l'introduction dans l'Union de lots de certains produits d'origine domestique solipèdes destinés à la consommation humaine et à certaines catégories d'équidés
Tableaux et figures
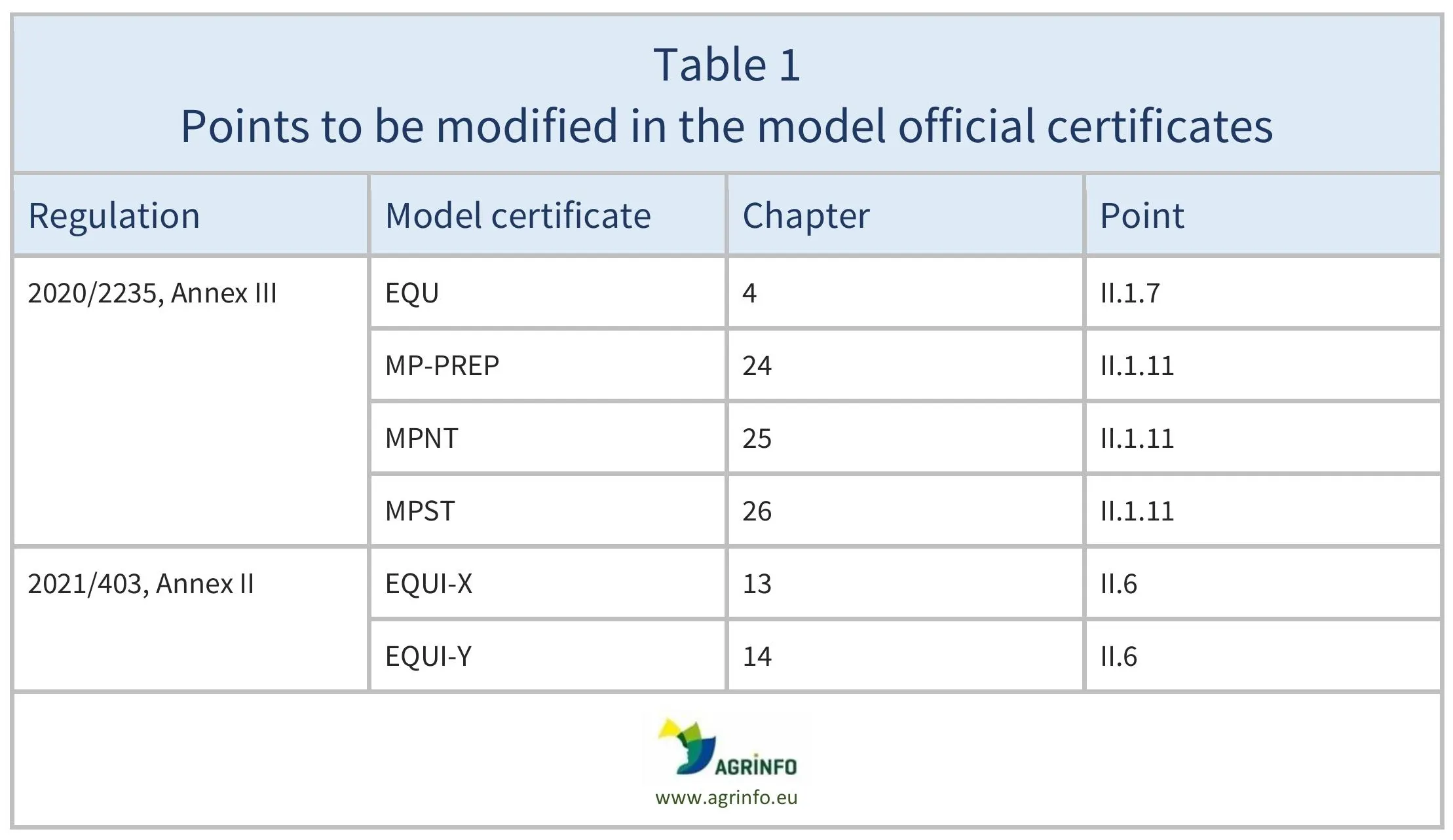
Source: Draft Regulation and Draft Annexes
Clause de non-responsabilité : COLEAD ne peut en aucun cas être tenu responsable des pertes, dommages, responsabilités ou dépenses encourus ou subis qui résulteraient de l'utilisation des informations disponibles sur ce site web ou de tout lien vers des sites externes. L'utilisation du site web se fait aux seuls risques et responsabilités de l'utilisateur. Cette plateforme d'information a été créée et maintenue avec le soutien financier de l'Union européenne. Son contenu ne reflète toutefois pas le point de vue de l'Union européenne.
L'UE va proposer des certificats sanitaires officiels révisés pour les chevaux producteurs de denrées alimentaires et les produits équins
Draft Commission Implementing Regulation as regards model certificates for entry into the Union of consignments of certain products of domestic solipeds origin intended for human consumption and certain categories of equine animals
qu'est-ce qui change et pourquoi ?
L'Union européenne (UE) interdit l'utilisation de certaines substances, telles que les substances thyréostatiques (antithyroïdiennes) et les stilbènes, au cours de la vie d'un cheval si la viande de ce cheval est destinée à être consommée comme denrée alimentaire dans l'UE. Les pays non membres de l'UE impliqués dans la production de viande de cheval doivent être répertoriés dans le règlement 2021/405, annexe I.
Le libellé des certificats officiels qui doivent accompagner les lots de ces produits ne reflète actuellement ces exigences que pour le pays exportateur ; il n'inclut pas les pays non membres de l'UE dans lesquels le cheval est né et a été élevé, s'ils sont différents du pays exportateur. Ce projet de règlement vise à aligner le libellé des certificats de sorte que les exigences s'appliquent non seulement au pays exportateur, mais aussi à tout pays tiers dans lequel le cheval est né ou a été élevé (s'il est différent) - comme décrit dans le tableau 1.
Actions
Lorsqu'un pays tiers exporte des chevaux ou leurs produits originaires d'un autre pays tiers, le vétérinaire officiel qui signe le certificat d'exportation doit vérifier que ce pays tiers supplémentaire respecte pleinement les règles de l'UE (y compris la non-utilisation de substances interdites) et figure avec un "X" pour "équins" à l'annexe I du règlement 2021/405.
La consultation de l'Organisation mondiale du commerce (OMC) a été clôturée le 30 décembre 2025.
Calendrier
Les certificats modifiés devraient s'appliquer à partir du 30 octobre 2026.
Tableaux et figures

Source: Draft Regulation and Draft Annexes
Clause de non-responsabilité : COLEAD ne peut en aucun cas être tenu responsable des pertes, dommages, responsabilités ou dépenses encourus ou subis qui résulteraient de l'utilisation des informations disponibles sur ce site web ou de tout lien vers des sites externes. L'utilisation du site web se fait aux seuls risques et responsabilités de l'utilisateur. Cette plateforme d'information a été créée et maintenue avec le soutien financier de l'Union européenne. Son contenu ne reflète toutefois pas le point de vue de l'Union européenne.
