Últimas autorizaciones, modificaciones y ampliaciones de nuevos alimentos 2024
- Food safety
- Novel/traditional foods
Resumen
Este informe resume las decisiones recientes de la UE para autorizar, modificar o ampliar las especificaciones o condiciones de uso de los nuevos alimentos existentes:
- 2'-FL obtenido por fermentación microbiana utilizando una cepa derivada de Escherichia coli por Kyowa Hakko Bio Co.
- Mezcla LNFP-I/2'-FL obtenida por fermentación microbiana utilizando una cepa derivada de E. coli
- Aceite deSchizochytrium limacinum (TKD-1)
- Aceite deSchizochytrium sp. (CABIO-A-2)
- Zumo de tallo de ashitaba.
La UE ha autorizado los siguientes cambios
- ampliación del uso del nuevo alimento biomasa de levadura Yarrowia lipolytica a los sustitutos de las comidas para el control del peso destinados a la población adulta
- requisitos de etiquetado "Proteína parcialmente hidrolizada de cebada y arroz" para alimentos que contengan proteína parcialmente hidrolizada de cebada y arroz usados
- las especificaciones y condiciones de uso del extracto proteico de riñones de cerdo sólo harán referencia a los niveles máximos autorizados; sus diferentes formas se eliminan de las especificaciones
- niveles más bajos de ácido docosahexaenoico (DHA) en las especificaciones del nuevo alimento Schizochytrium sp. aceite rico en DHA y ácido eicosapentaenoico (EPA)
- los niveles autorizados de 2'-FL aumentarán con respecto a los niveles actuales autorizados tanto en los preparados para lactantes como en los preparados de continuación
- los niveles autorizados de endotoxinas residuales para el 2'-FL producido a partir de la cepa derivada E. coli BL-21 se alinearán con los niveles ya autorizados en las mismas condiciones de uso para el 2'-FL de E. coli K-12, y otros oligosacáridos lácteos en niveles residuales similares en preparados para lactantes y preparados de continuación.
Nuevas autorizaciones alimentarias, usos modificados y prórrogas adoptadas de enero a julio de 2024
Autorizaciones
Reglamentos de aplicación de la Comisión 2024/2036, 2024/2049, 2024/2061, 2024/2090, 2024/2101
Enmiendas
Reglamentos de aplicación de la Comisión 2024/2044, 2024/2046, 2024/2048, 2024/2062, 2024/2102
Actualización
Este informe resume las decisiones recientes de la UE para autorizar, modificar o ampliar las especificaciones o condiciones de uso de los nuevos alimentos existentes:
- 2'-FL obtenido por fermentación microbiana utilizando una cepa derivada de Escherichia coli por Kyowa Hakko Bio Co.
- Mezcla LNFP-I/2'-FL obtenida por fermentación microbiana utilizando una cepa derivada de E. coli
- Aceite deSchizochytrium limacinum (TKD-1)
- Aceite deSchizochytrium sp. (CABIO-A-2)
- Zumo de tallo de ashitaba.
La UE ha autorizado los siguientes cambios
- ampliación del uso del nuevo alimento biomasa de levadura Yarrowia lipolytica a los sustitutos de las comidas para el control del peso destinados a la población adulta
- requisitos de etiquetado "Proteína parcialmente hidrolizada de cebada y arroz" para alimentos que contengan proteína parcialmente hidrolizada de cebada y arroz usados
- las especificaciones y condiciones de uso del extracto proteico de riñones de cerdo sólo harán referencia a los niveles máximos autorizados; sus diferentes formas se eliminan de las especificaciones
- niveles más bajos de ácido docosahexaenoico (DHA) en las especificaciones del nuevo alimento Schizochytrium sp. aceite rico en DHA y ácido eicosapentaenoico (EPA)
- los niveles autorizados de 2'-FL aumentarán con respecto a los niveles actuales autorizados tanto en los preparados para lactantes como en los preparados de continuación
- los niveles autorizados de endotoxinas residuales para el 2'-FL producido a partir de la cepa derivada E. coli BL-21 se alinearán con los niveles ya autorizados en las mismas condiciones de uso para el 2'-FL de E. coli K-12, y otros oligosacáridos lácteos en niveles residuales similares en preparados para lactantes y preparados de continuación.
Productos afectados
Productos lácteos (pasteurizados, esterilizados, UHT), productos lácteos fermentados, bebidas aromatizadas, barritas de cereales, preparados para lactantes, preparados de continuación, alimentos elaborados a base de cereales y alimentos infantiles, alimentos dietéticos sustitutivos (para control de peso), alimentos médicos especiales, complementos alimenticios
¿qué está cambiando?
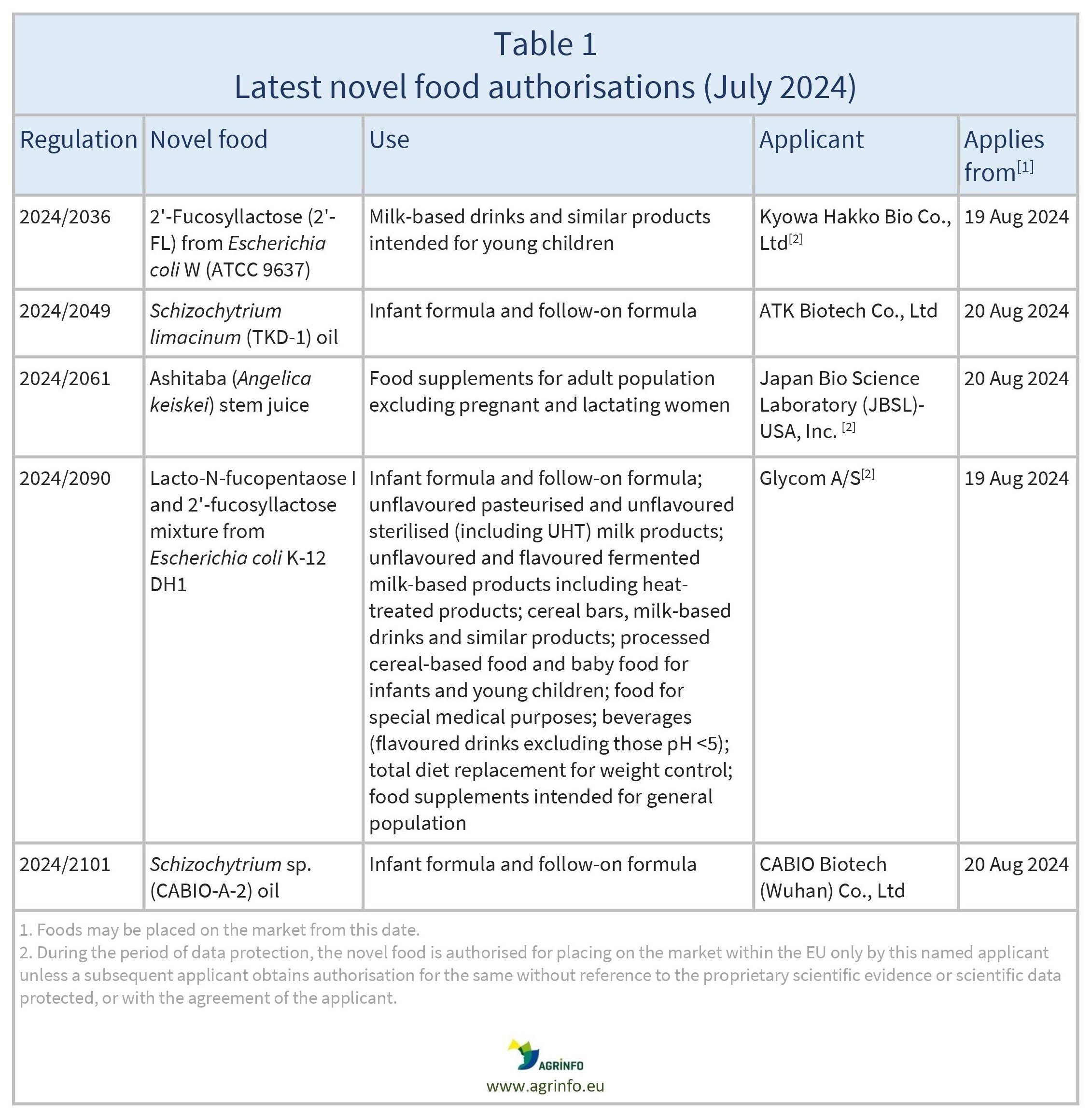
La Comisión Europea ha autorizado la comercialización en la UE de los nuevos alimentos enumerados en el cuadro 1. Estos alimentos se incluirán en la lista de nuevos alimentos de la Unión (Reglamento 2017/2470). En el caso de determinados nuevos alimentos, solo las empresas solicitantes a las que se concedió la autorización podrán venderlos en el mercado de la UE durante los próximos 5 años, a menos que permitan que otras empresas los vendan, o si otra empresa obtiene una autorización de nuevo alimento sin hacer referencia a los datos científicos protegidos utilizados por el solicitante original (véase la nota a pie de página del cuadro 1).
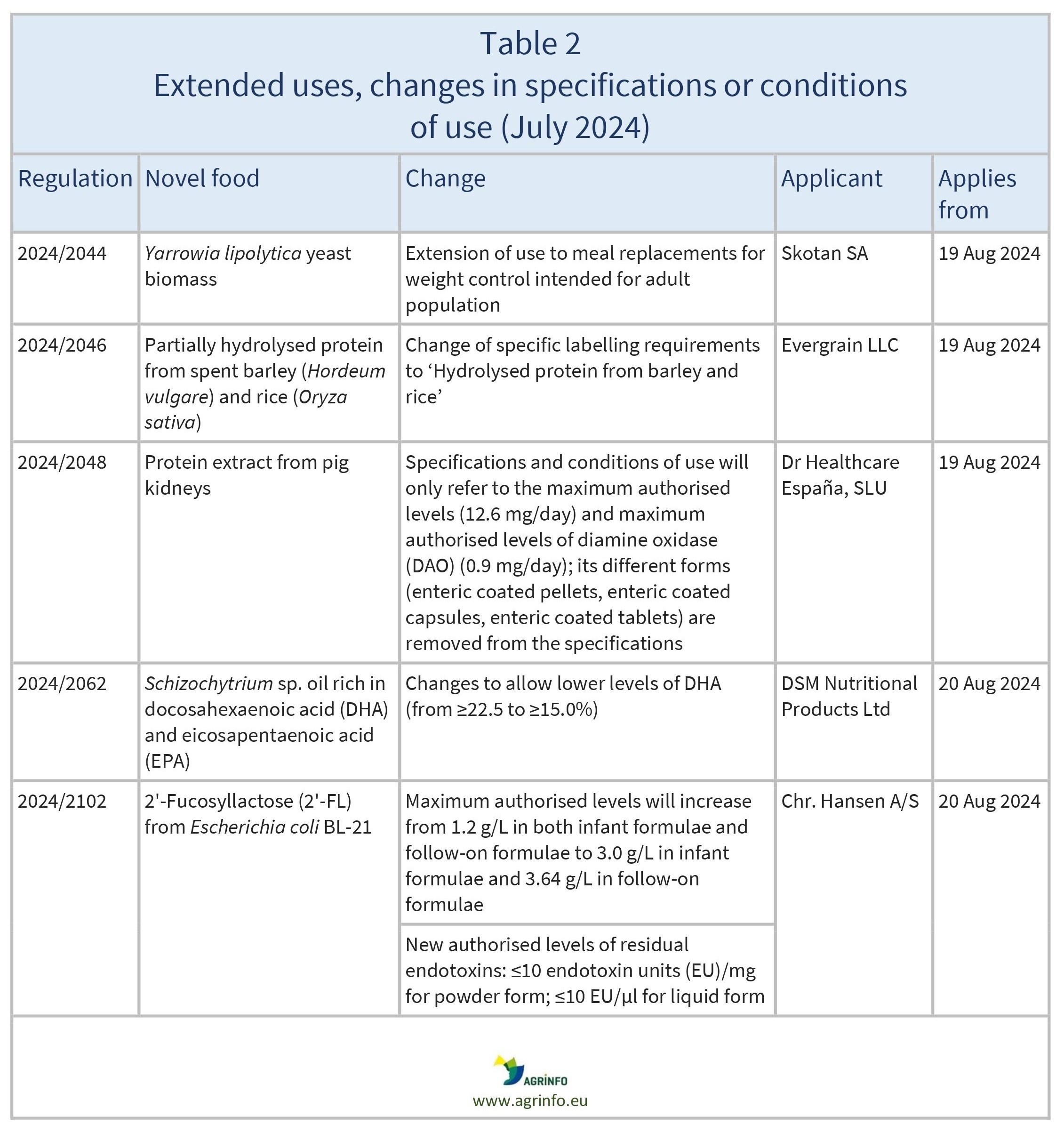
La Comisión también ha autorizado algunos cambios en las especificaciones y condiciones de uso de determinados nuevos alimentos ya autorizados y disponibles en el mercado de la UE (véase el cuadro 2).
¿Por qué?
Solo los nuevos alimentos autorizados e incluidos en la lista de la Unión de nuevos alimentos pueden comercializarse en la UE (Reglamento 2015/2283).
La Autoridad Europea de Seguridad Alimentaria (EFSA) evalúa las solicitudes de nuevos alimentos para garantizar su seguridad en las condiciones y/o niveles de uso propuestos [véanse los Recursos 1-6].
Cronología
Los nuevos alimentos recientemente autorizados podrán comercializarse en la UE a partir de la fecha indicada en el cuadro 1.
Las modificaciones de las especificaciones y condiciones se aplican a partir de las fechas indicadas en el cuadro 2.
Antecedentes
Para más información sobre el proceso de autorización de nuevos alimentos, véase Explicación de los nuevos alimentos.
Recursos
Comisión Europea: Lista de la Unión de nuevos alimentos
Reglamento (UE) 2017/2470 (lista de la Unión de nuevos alimentos)
Reglamento (UE) 2015/2283 sobre nuevos alimentos
Reglamento nº 1169/2011 sobre la información alimentaria facilitada al consumidor
Dictámenes publicados por la Autoridad Europea de Seguridad Alimentaria (EFSA) sobre la seguridad/eficacia de los siguientes nuevos alimentos:
- EFSA (2023) Seguridad de la 2′-fucosilactosa (2′-FL) producida por una cepa derivada (Escherichia coli SGR5) de E. coli W (ATCC 9637) como nuevo alimento de conformidad con el Reglamento (UE) 2015/2283. EFSA Journal, 21(11): 8333.
- EFSA (2023) Seguridad de la ampliación del uso de 2′-fucosilactosa (2′-FL) como nuevo alimento de conformidad con el Reglamento (UE) 2015/2283. EFSA Journal, 21(11): e8334.
- EFSA (2023) Safety of an extension of use of Yarrowia lipolytica yeast biomass as a novel food pursuant to Regulation (EU) 2015/2283. EFSA Journal, 21(11): e8416.
- EFSA (2023) Seguridad de la mezcla de lacto-N-fucopentaosa I/2'-fucosilactosa (LNFP-I/2'-FL) como nuevo alimento de conformidad con el Reglamento (UE) 2015/2283. EFSA Journal, 21(12): e8412.
- EFSA (2023) Seguridad del aceite de Schizochytrium limacinum (cepa TKD-1) para su uso en preparados para lactantes y preparados de continuación como nuevo alimento de conformidad con el Reglamento (UE) 2015/2283. EFSA Journal, 21(12): e8414.
- EFSA (2023) Seguridad del aceite de Schizochytrium sp. (cepa CABIO-A-2) para su uso en preparados para lactantes y preparados de continuación como nuevo alimento de conformidad con el Reglamento (UE) 2015/2283. EFSA Journal, 21(12): e8415.
Fuentes
Reglamento de aplicación de la Comisión:
2024/2036 por el que se autoriza la comercialización de 2'-Fucosilactosa producida por una cepa derivada de Escherichia coli W (ATCC 9637) como nuevo alimento
2024/2044 en lo que respecta a las especificaciones y las condiciones de uso del nuevo alimento biomasa de levadura Yarrowia lipolytica
2024/2046 por lo que se refiere a los requisitos específicos de etiquetado del nuevo alimento proteína parcialmente hidrolizada de cebada(Hordeum vulgare) y arroz(Oryza sativa) usados
2024/2048 por lo que se refiere a las especificaciones y las condiciones de uso del nuevo extracto proteico alimentario de riñones de cerdo
2024/2049 por la que se autoriza la comercialización de aceite de Schizochytrium limacinum (TKD-1) como nuevo alimento
2024/2061 por la que se autoriza la comercialización del zumo de los tallos de la planta Angelica keiskei (zumo de tallos de ashitaba) como nuevo alimento
2024/2062 relativa a las especificaciones del nuevo alimento aceite de Schizochytrium sp. rico en DHA y EPA
2024/2090 por la que se autoriza la comercialización de la mezcla de lacto-N-fucopentaosa I y 2'-fucosilactosa producida utilizando una cepa derivada de Escherichia coli K-12 DH1 como nuevo alimento
2024/2101 por la que se autoriza la comercialización de aceite de Schizochytrium sp. (CABIO-A-2) como nuevo alimento
2024/2102 por lo que se refiere a las condiciones de uso del nuevo alimento 2'-Fucosilactosa y a las especificaciones del nuevo alimento 2'-Fucosilactosa producido con una cepa derivada de Escherichia coli BL-21
Descargo de responsabilidad: COLEAD no se hace responsable de ninguna pérdida, daño, responsabilidad o gasto incurrido o sufrido como resultado de la utilización de la información disponible en este sitio web o de cualquier enlace a sitios externos. El uso del sitio web es por cuenta y riesgo exclusivo del usuario. Esta plataforma de información ha sido elaborada y mantenida con el apoyo financiero de la Unión Europea. No obstante, su contenido no refleja las opiniones de la Unión Europea.
Nuevas autorizaciones alimentarias, usos modificados y prórrogas adoptadas de enero a julio de 2024
Authorisations
Commission Implementing Regulations 2024/2036, 2024/2049, 2024/2061, 2024/2090, 2024/2101
Amendments
Commission Implementing Regulations 2024/2044, 2024/2046, 2024/2048, 2024/2062, 2024/2102
¿qué está cambiando y por qué?
La Comisión Europea ha autorizado la comercialización en la UE de los nuevos alimentos enumerados en el cuadro 1.
La Comisión también ha autorizado algunos cambios en las especificaciones y condiciones de uso de determinados nuevos alimentos que ya están autorizados y disponibles en el mercado de la UE (véase el cuadro 2).
Cronología
Los nuevos alimentos recientemente autorizados podrán comercializarse en la UE a partir de la fecha indicada en el cuadro 1.
Las modificaciones de las especificaciones y condiciones se aplican a partir de las fechas indicadas en el cuadro 2.
Tablas y figuras
Descargo de responsabilidad: COLEAD no se hace responsable de ninguna pérdida, daño, responsabilidad o gasto incurrido o sufrido como resultado de la utilización de la información disponible en este sitio web o de cualquier enlace a sitios externos. El uso del sitio web es por cuenta y riesgo exclusivo del usuario. Esta plataforma de información ha sido elaborada y mantenida con el apoyo financiero de la Unión Europea. No obstante, su contenido no refleja las opiniones de la Unión Europea.